La parte más importante para entender los aminoácidos es la cadena lateral. La cadena lateral también se denomina grupo R y es la parte que difiere entre los aminoácidos. Aunque los aminoácidos comparten un esqueleto común, al cambiar el grupo R cambian propiedades como la solubilidad en agua, la carga y la tendencia a quedar en el interior de una proteína. NCBI Bookshelf explica que los aminoácidos tienen un grupo α-carboxilo, un grupo α-amino y un grupo R, y que las diferencias en el grupo R determinan las propiedades únicas de cada aminoácido.
La estructura básica de un aminoácido se puede representar de la siguiente manera.
H2N-CH(R)-COOH
Conceptos básicos de la cadena lateral: ejemplos de grupos R
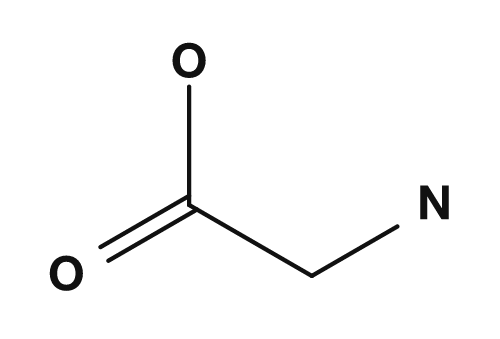
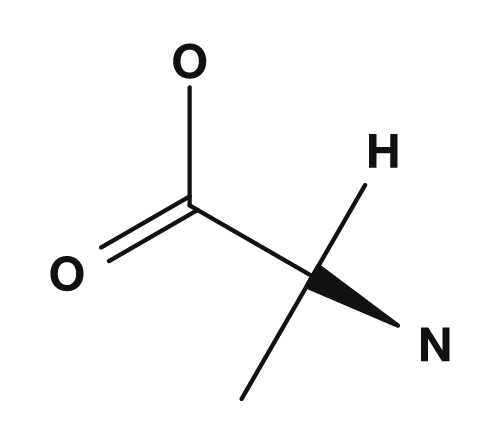
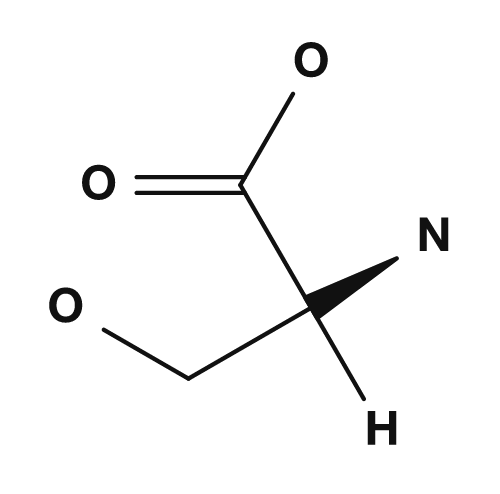
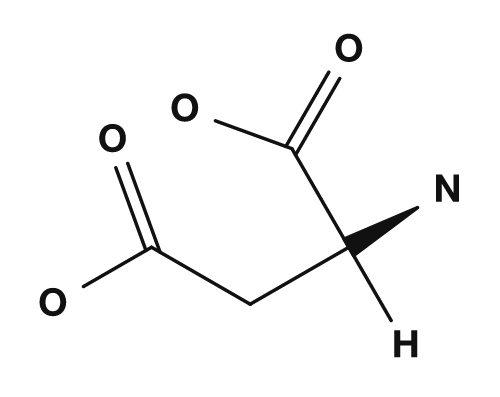
La parte R es la cadena lateral. Por ejemplo, en la glicina el grupo R es un átomo de hidrógeno, en la alanina es un grupo metilo, en la serina es un grupo hidroximetilo y en el ácido aspártico es un grupo carboximetilo. Estas pequeñas diferencias tienen un gran impacto en las propiedades del aminoácido.
| Aminoácido | Grupo R | Características |
|---|---|---|
| Glicina | Hidrógeno | El aminoácido más pequeño, aquiral |
| Alanina | Grupo metilo | Apolar simple |
| Serina | Grupo hidroximetilo | Polar, participa en enlaces de hidrógeno |
| Ácido aspártico | Grupo carboximetilo | Ácido, suele tener carga negativa |
| Glicina | Alanina | Serina | Ácido aspártico |
|---|---|---|---|
|
|
|
|
Afinidad por el agua: hidrofóbico e hidrofílico
La forma más fundamental de clasificar las cadenas laterales es según su afinidad por el agua.
- Las cadenas laterales que contienen muchos hidrocarburos tienden a ser hidrofóbicas y a agruparse en el interior de la proteína.
- Las cadenas laterales que contienen oxígeno o nitrógeno suelen participar en enlaces de hidrógeno y, por tanto, son hidrofílicas.
La forma de una proteína está muy influenciada por estas interacciones entre cadenas laterales. Molecular Biology of the Cell de NCBI Bookshelf explica que los aminoácidos con cadenas laterales hidrofóbicas tienden a agruparse en el interior de la proteína y que las interacciones no covalentes estabilizan la estructura plegada.
Cadenas laterales ácidas y básicas
El siguiente punto importante son las cadenas laterales ácidas y básicas.
El ácido aspártico y el ácido glutámico tienen grupos carboxilo en su cadena lateral y tienden a tener una carga negativa al pH fisiológico. La lisina, la arginina y la histidina tienen nitrógeno básico en su cadena lateral. En particular, la lisina y la arginina tienden a tener carga positiva, y la histidina es importante como cadena lateral que se protona fácilmente según las condiciones. Un artículo publicado en PMC también explica que, cerca del pH neutro, el ácido aspártico y el ácido glutámico tienen carga negativa, y la lisina, la arginina y la histidina se tratan como aminoácidos implicados en el estado de carga.
| Carga | Aminoácidos representativos | Grupos funcionales en la cadena lateral |
|---|---|---|
| Negativa (ácida) | Ácido aspártico, ácido glutámico | Grupo carboxilo |
| Positiva (básica) | Lisina, arginina, histidina | Grupo amino, grupo guanidino, imidazol |
| Lisina | Fenilalanina | Cisteína |
|---|---|---|
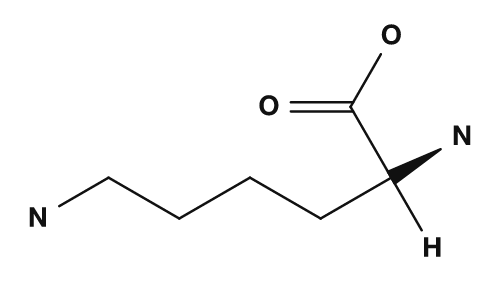
|
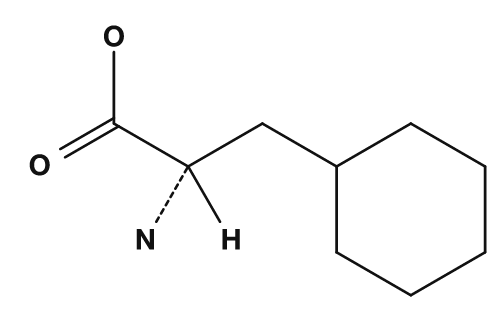
|
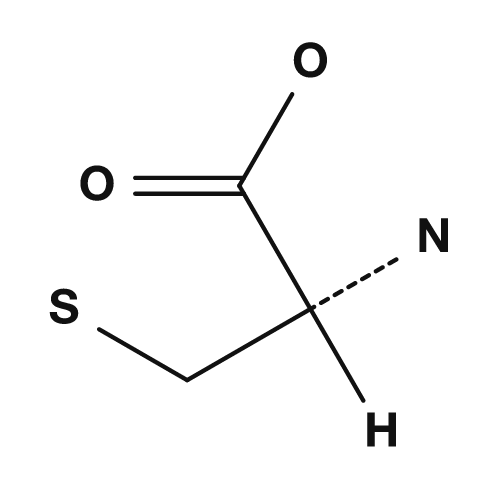
|
Cadenas laterales aromáticas
Entre los aminoácidos con cadenas laterales aromáticas se encuentran la fenilalanina, la tirosina y el triptófano. Estos tienen sistemas de electrones π cíclicos y son relativamente fáciles de identificar en las fórmulas estructurales. La tirosina posee un grupo hidroxilo fenólico, por lo que muestra propiedades distintas de un simple aromático hidrofóbico. El triptófano tiene un gran anillo indol y es importante también desde el punto de vista de la estructura proteica y la absorción de luz.
Cadenas laterales que contienen azufre
También merecen atención las cadenas laterales que contienen azufre.
La cisteína tiene un grupo tiol (-SH), y cuando dos cisteínas se oxidan, pueden formar un enlace disulfuro. Este es un enlace importante que estabiliza la estructura tridimensional de las proteínas. La metionina tiene una estructura de tioéter y también es bien conocida como el aminoácido correspondiente al codón de inicio AUG de la traducción.
| Tipo de cadena lateral | Aminoácidos representativos | Puntos clave |
|---|---|---|
| Hidrofóbica | Valina, leucina, isoleucina | Tienden a agruparse en el interior de las proteínas |
| Aromática | Fenilalanina, tirosina, triptófano | Sistema de electrones π, implicado en la absorción UV |
| Que contiene azufre | Cisteína, metionina | Enlaces disulfuro, relación con el codón de inicio AUG |
Cómo leer las fórmulas estructurales
Al estudiar las cadenas laterales, es más fácil entender si se piensa a partir de la fórmula estructural en lugar de memorizar por separado los nombres de los aminoácidos y sus propiedades.
- Tiene oxígeno o nitrógeno → tiende a ser polar
- Tiene un grupo carboxilo → tiende a ser ácido
- Tiene un grupo amino o guanidino → tiende a ser básico
- Tiene muchos hidrocarburos → tiende a ser hidrofóbico
Resumen
La cadena lateral de un aminoácido es la parte clave que determina sus propiedades. Las diferencias en el grupo R dan lugar a características como hidrofobicidad, hidrofilicidad, acidez, basicidad, aromaticidad y contenido de azufre. Al observar las fórmulas estructurales, prestar atención no solo al esqueleto común, sino también a qué átomos y grupos funcionales hay en la cadena lateral, facilita mucho la comprensión de las propiedades de los aminoácidos.