Los aminoácidos cambian su estado de carga según el pH. En condiciones ácidas tienden a tener una carga positiva, y en condiciones básicas, una carga negativa. El punto isoeléctrico es clave para comprender estos cambios de carga. El punto isoeléctrico puede entenderse como el pH al que la carga neta de la molécula se vuelve cero, con cargas positivas y negativas en equilibrio. El IUPAC Gold Book describe el estado isoeléctrico como la condición en la que un poliamfolito, especialmente una proteína, no muestra electroforesis.
pH y Cambios de Carga
La estructura básica de los aminoácidos incluye un grupo amino y un grupo carboxilo.
- En condiciones ácidas, el grupo amino tiende a aceptar un protón y convertirse en
-NH3+, mientras que el grupo carboxilo tiende a adoptar la forma-COOH. - En condiciones básicas, el grupo carboxilo pierde un protón y se convierte en
-COO-, y el grupo amino se aproxima al estado-NH2. - A pH intermedio, predomina la forma con tanto
-NH3+como-COO-(zwitterion).
| Condición de pH | Estado del grupo amino | Estado del grupo carboxilo | Carga neta |
|---|---|---|---|
| Ácido (pH bajo) | -NH3+ (positivo) |
-COOH (neutro) |
Positiva |
| Cerca del punto isoeléctrico | -NH3+ (positivo) |
-COO- (negativo) |
0 (zwitterion) |
| Básico (pH alto) | -NH2 (neutro) |
-COO- (negativo) |
Negativa |
¿Qué Es el Punto Isoeléctrico?
Tomando como ejemplo la glicina, el aminoácido más simple: en el lado ácido tiende a tener una carga positiva global, y en el básico, una negativa. En algún punto intermedio, hay un pH en el que la carga neta se vuelve cero. Ese es el punto isoeléctrico de la glicina.
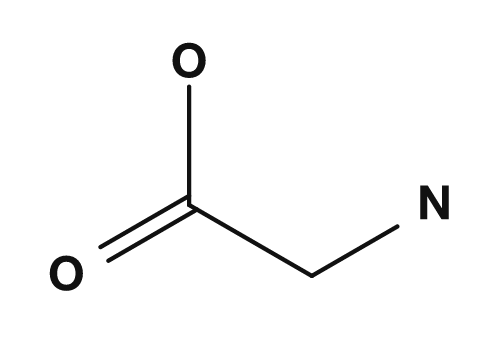
Al comprender el punto isoeléctrico, es más preciso pensarlo como un estado donde las cargas positivas y negativas están equilibradas, en lugar de un estado sin cargas. Los aminoácidos tienden a existir como zwitteriones cerca del pH neutro, llevando tanto cargas positivas como negativas dentro de la molécula. PubChem explica que el zwitterion de L-cisteinilglicina surge de la transferencia de un protón de un grupo hidroxi a un grupo amino, y es la microespecie principal a pH 7,3.
Cómo las Cadenas Laterales Afectan al Punto Isoeléctrico
El punto isoeléctrico varía según el tipo de cadena lateral.
- El ácido aspártico y el ácido glutámico, que tienen grupos carboxilo en sus cadenas laterales, tienden a tener una carga negativa, por lo que sus puntos isoeléctricos son más bajos.
- Los aminoácidos con cadenas laterales básicas, como la lisina y la arginina, tienden a tener una carga positiva, por lo que sus puntos isoeléctricos son más altos.
Un artículo de PMC explica que el pI de una proteína se define como el pH al que la carga neta es cero, y depende fuertemente de la composición de aminoácidos y los valores de pKa de cada cadena lateral.
| Naturaleza de la cadena lateral | Aminoácidos representativos | Efecto en el punto isoeléctrico |
|---|---|---|
| Cadena lateral con grupo carboxilo (ácido) | Ácido aspártico, Ácido glutámico | Disminuye el punto isoeléctrico |
| Cadena lateral con nitrógeno básico (básico) | Lisina, Arginina, Histidina | Aumenta el punto isoeléctrico |
| Ácido aspártico | Ácido glutámico | Lisina |
|---|---|---|
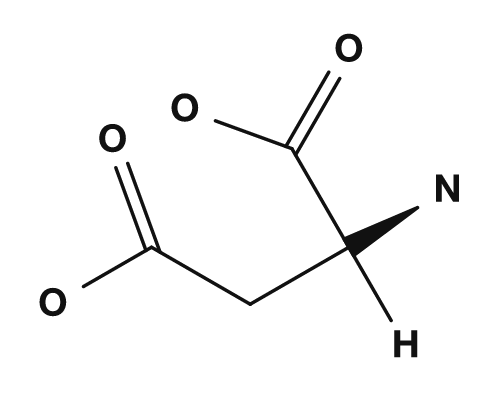
|
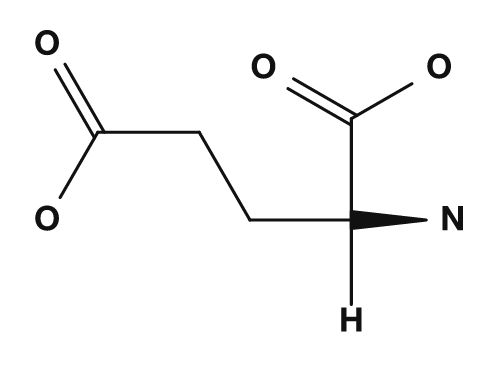
|
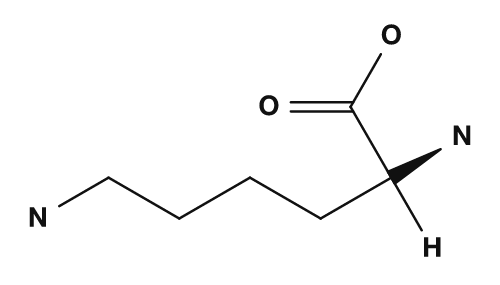
|
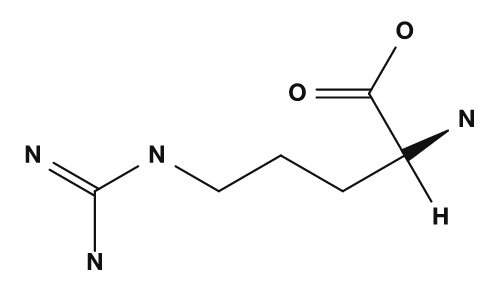
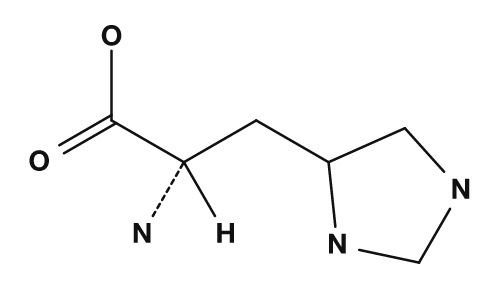
| Arginina | Histidina |
|---|---|
|
|
Pensar en la Carga desde las Fórmulas Estructurales
Al pensar en el punto isoeléctrico desde las fórmulas estructurales, el primer paso es buscar partes que puedan llevar una carga.
- Identificar el grupo amino y el grupo carboxilo
- Verificar si la cadena lateral tiene grupos funcionales ácidos o básicos
- Ácido aspártico y ácido glutámico → grupo carboxilo en la cadena lateral
- Lisina → grupo amino en la cadena lateral
- Arginina → grupo guanidino
- Histidina → anillo imidazol
Aplicaciones del Punto Isoeléctrico
El punto isoeléctrico también es importante en la separación y purificación de proteínas. Dado que la carga neta de una molécula cambia con el pH, se utiliza en electroforesis y cromatografía de intercambio iónico.
- Cuando el pH está por debajo del punto isoeléctrico → la molécula tiende a estar cargada positivamente
- Cuando el pH está por encima del punto isoeléctrico → la molécula tiende a estar cargada negativamente
Un artículo de PMC también establece que las proteínas llevan carga positiva a pH por debajo del pI y carga negativa a pH por encima del pI.
Resumen
El punto isoeléctrico es el pH al que la carga neta de un aminoácido o proteína se vuelve cero. En los aminoácidos, los estados de ionización del grupo amino, el grupo carboxilo y la cadena lateral cambian con el pH, por lo que la carga también cambia. Al leer fórmulas estructurales, buscar grupos funcionales que puedan llevar una carga es el primer paso para comprender el punto isoeléctrico.