La mayoría de los aminoácidos tienen estereoisómeros. Esto se debe a que el carbono α actúa como un centro quiral. Un centro quiral es un átomo de carbono unido a cuatro sustituyentes diferentes. En la mayoría de los α-aminoácidos que forman proteínas, el carbono α está unido a un grupo amino, un grupo carboxilo, un átomo de hidrógeno y un grupo lateral R, lo que lo convierte en un centro quiral. NCBI Bookshelf explica que los aminoácidos que forman proteínas son α-aminoácidos, y todos excepto la glicina tienen un centro quiral en el carbono α.
Notación D y L
Una notación común en la estereoquímica de aminoácidos es la forma D y la forma L. La notación D/L representa la configuración relativa tomando el gliceraldehído como referencia. Los aminoácidos estándar que componen las proteínas son fundamentalmente L-aminoácidos. NCBI Bookshelf también afirma que los 20 aminoácidos en proteínas son el L-isómero.
Diferencia Entre la Notación D/L y la Notación R/S
La notación D/L y la notación R/S no son lo mismo.
| Sistema de notación | Base | Aminoácidos que forman proteínas | Excepciones |
|---|---|---|---|
| Notación D/L | Configuración relativa basada en el gliceraldehído | Forma L | Glicina (sin centro quiral) |
| Notación R/S | Configuración absoluta por reglas de prioridad CIP | Principalmente configuración S | Cisteína (configuración R) |
D/L es una notación basada en la configuración relativa histórica, mientras que R/S es una configuración absoluta basada en las reglas de prioridad CIP. La mayoría de los L-aminoácidos tienen configuración S, pero la cisteína es una excepción: su cadena lateral contiene azufre, lo que cambia el orden de prioridad y le da la configuración R. NCBI Bookshelf también indica que los aminoácidos estándar, excepto glicina y cisteína, tienen configuración S en la notación R/S, mientras que la cisteína tiene configuración R debido a su grupo R que contiene azufre.
Identificación de Centros Quirales en Fórmulas Estructurales
Cuando se busca un centro quiral en una fórmula estructural, hay que centrarse en el carbono α. Si los cuatro sustituyentes unidos a ese carbono son todos diferentes, es un centro quiral.
| Aminoácido | Sustituyentes en el carbono α | Centro quiral |
|---|---|---|
| Alanina | NH2, COOH, H, CH3 |
Sí (los cuatro son diferentes) |
| Glicina | NH2, COOH, H, H |
No (dos hidrógenos) |
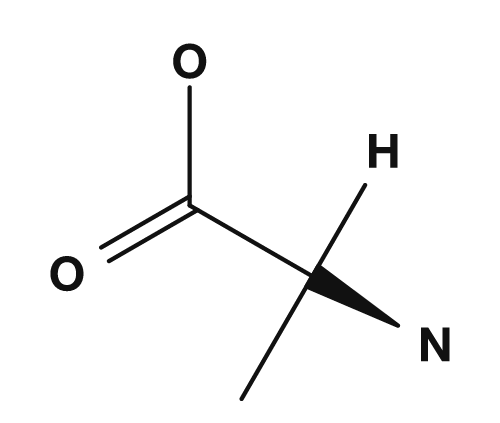
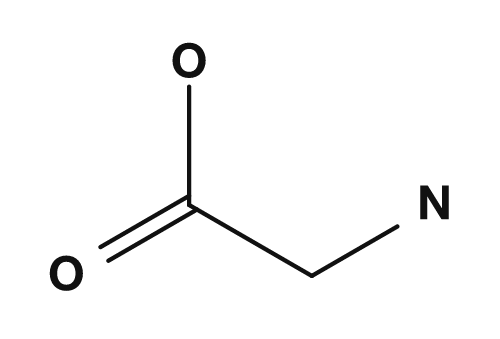
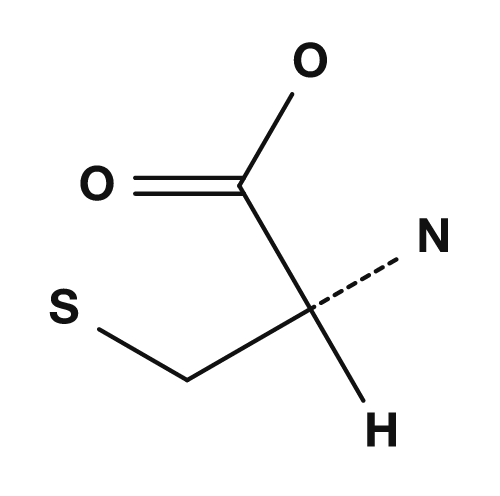
| Alanina | Glicina | Cisteína |
|---|---|---|
|
|
|
En la alanina, el carbono α está unido a NH2, COOH, H y CH3. Dado que los cuatro son diferentes, la alanina es quiral. En la glicina, el grupo R es hidrógeno, por lo que el carbono α está unido a NH2, COOH, H y H — solo hay tres sustituyentes distintos, por lo que no tiene centro quiral. PubChem también indica que la glicina, con un átomo de hidrógeno como cadena lateral, es el único aminoácido proteico aquiral.
Formas D y L y Rotación Óptica
Las formas D y L están relacionadas como enantiómeros (imágenes especulares). Cuando dos moléculas con la misma fórmula molecular y las mismas relaciones de enlace no pueden superponerse a sus imágenes especulares, se denominan enantiómeros. En los aminoácidos, esta diferencia en la configuración espacial afecta enormemente las interacciones con biomoléculas. Dado que las enzimas y los receptores en los organismos vivos tienen estructuras tridimensionales, pueden distinguir entre las formas L y D.
Un punto importante al aprender la notación D/L para aminoácidos es no pensar simplemente que "L significa levógiro" o "D significa dextrógiro." La notación D/L no indica directamente la dirección de rotación óptica. La rotación óptica es una propiedad medida experimentalmente y se expresa como + o -. D/L es un símbolo que representa la configuración relativa estructural.
Puntos Clave para el Aprendizaje con Fórmulas Estructurales
Al aprender con fórmulas estructurales, el primer paso es verificar si el carbono α tiene cuatro sustituyentes diferentes.
- Verificar si el carbono α tiene cuatro sustituyentes diferentes
- La glicina es excepcionalmente sin centro quiral
- Los aminoácidos en proteínas son fundamentalmente forma L
- La notación D/L y la notación R/S son sistemas diferentes
- La cisteína es una excepción: forma L pero configuración R
Resumen
La mayoría de los aminoácidos son quirales porque el carbono α tiene cuatro sustituyentes diferentes. Los aminoácidos estándar en proteínas son fundamentalmente forma L, y solo la glicina carece de un centro quiral porque tiene dos átomos de hidrógeno idénticos en el carbono α. La notación D/L y la notación R/S son sistemas diferentes, y la cisteína en particular debe entenderse como una excepción.