Los aminoácidos representativos que forman las proteínas son 20. Todos comparten el mismo esqueleto básico, pero su cadena lateral (grupo R) es diferente. NCBI Bookshelf cita como los 20 aminoácidos proteinogénicos a la alanina, arginina, asparagina, ácido aspártico, cisteína, ácido glutámico, glutamina, glicina, histidina, isoleucina, leucina, lisina, metionina, fenilalanina, prolina, serina, treonina, triptófano, tirosina y valina.
Para aprender los 20 aminoácidos, es más fácil clasificarlos según las propiedades de la cadena lateral que memorizar los nombres de carrerilla.
Primero, aquí tiene un resumen de los 20.
| Categoría | Principales aminoácidos | Características de la cadena lateral |
|---|---|---|
| No polares | Glicina, alanina, valina, leucina, isoleucina, prolina, metionina | Tienden a no mezclarse con el agua |
| Polares (sin carga) | Serina, treonina, asparagina, glutamina | Suelen participar en enlaces de hidrógeno |
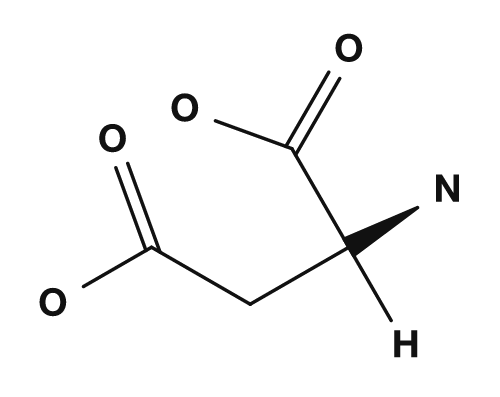
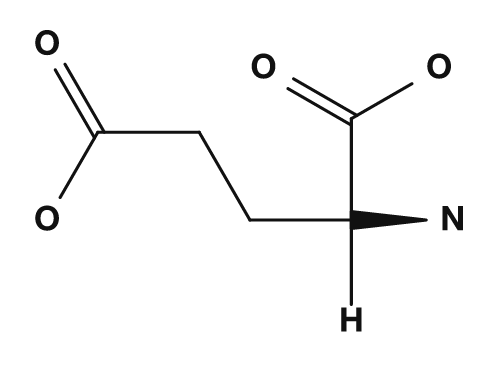
| Ácidos | Ácido aspártico, ácido glutámico | Carga negativa al pH fisiológico |
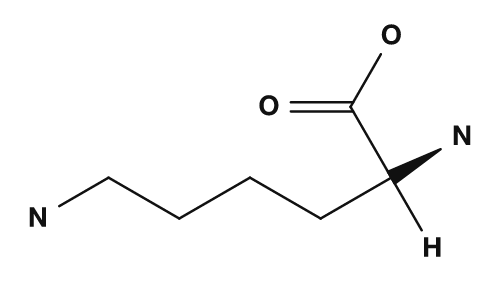
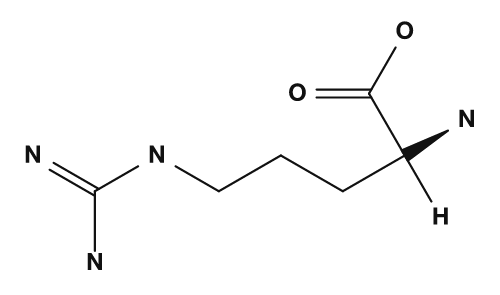
| Básicos | Lisina, arginina, histidina | Cadenas laterales básicas, propensas a tener carga positiva |
| Aromáticos | Fenilalanina, tirosina, triptófano | Poseen anillos aromáticos |
| Con azufre | Cisteína, metionina | Grupo tiol o tioéter |
| Estructura especial | Prolina | Amina secundaria, estructura cíclica |
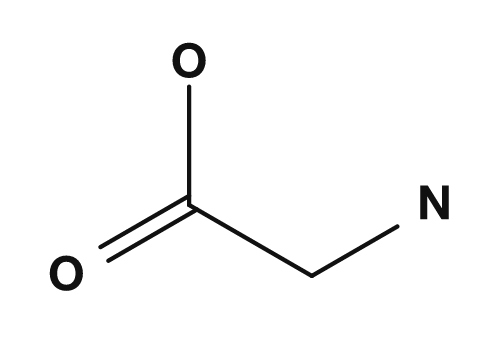
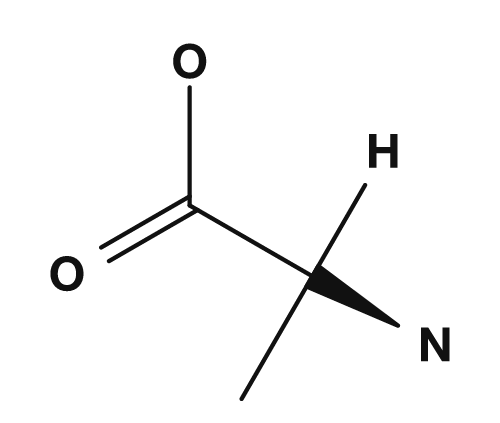
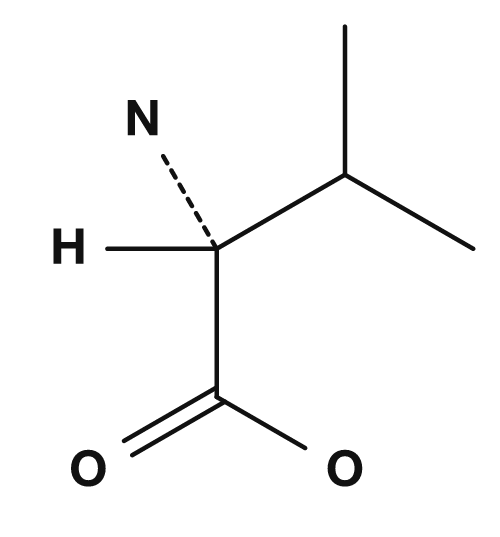
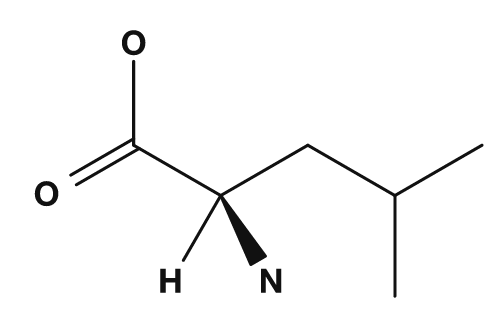
| Glicina | Alanina | Valina | Leucina | Isoleucina |
|---|---|---|---|---|
|
|
|
|
|
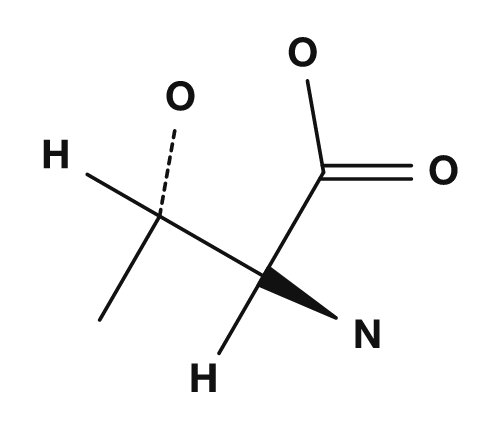
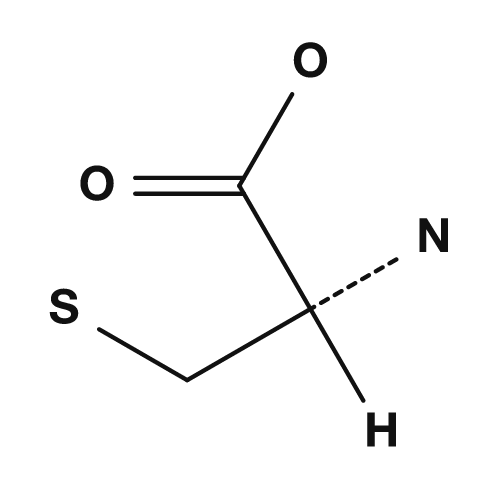
| Prolina | Metionina | Serina | Treonina | Cisteína |
|---|---|---|---|---|
|
|
|
|
|
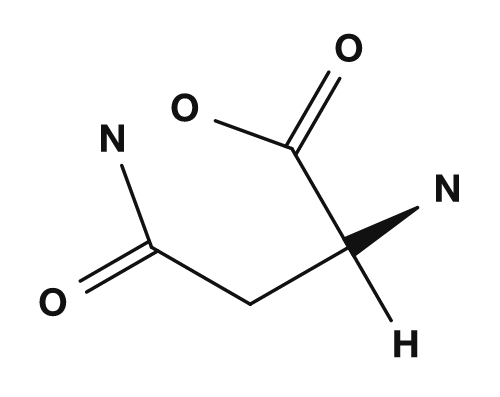
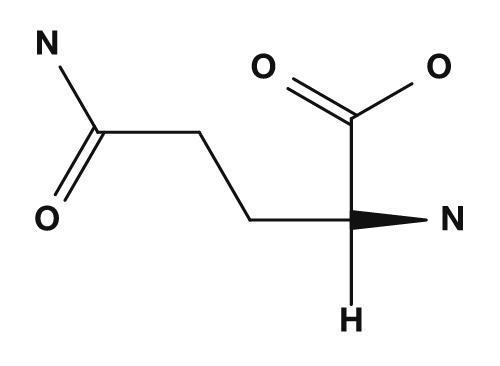
| Asparagina | Glutamina | Ácido aspártico | Ácido glutámico | Lisina |
|---|---|---|---|---|
|
|
|
|
|
| Arginina | Histidina | Fenilalanina | Tirosina | Triptófano |
|---|---|---|---|---|
|
|
|
|
|
Aminoácidos no polares
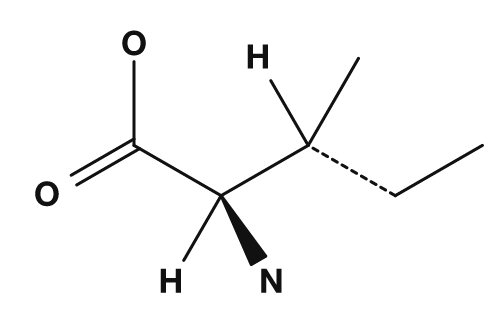
Entre los aminoácidos no polares se encuentran la glicina, alanina, valina, leucina, isoleucina, prolina y metionina. Estos tienen cadenas laterales que no se mezclan bien con el agua y tienden a agruparse en el interior de las proteínas. En particular, la valina, la leucina y la isoleucina también se conocen como aminoácidos de cadena ramificada.
Aminoácidos polares (sin carga)
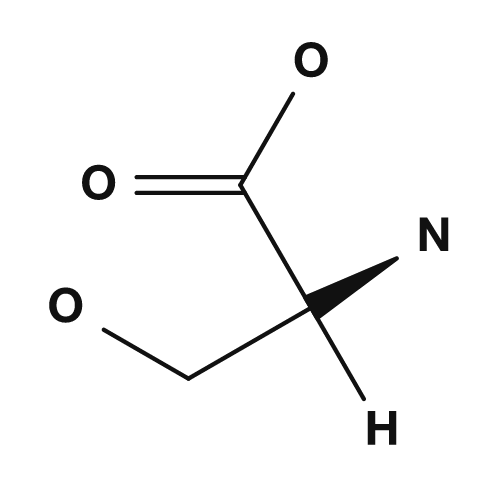
Como aminoácidos polares pero con poca tendencia a tener carga están la serina, treonina, asparagina y glutamina. Estos poseen cadenas laterales que contienen oxígeno o nitrógeno y pueden participar en enlaces de hidrógeno. Interactúan con el agua en la superficie de las proteínas y desempeñan un papel importante en los sitios activos de las enzimas.
Aminoácidos ácidos y básicos
Aminoácidos ácidos
Entre los aminoácidos ácidos están el ácido aspártico y el ácido glutámico. Estos tienen un grupo carboxilo en la cadena lateral y, al pH fisiológico, suelen llevar carga negativa.
Aminoácidos básicos
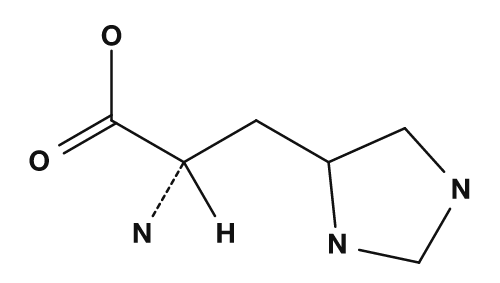
Entre los aminoácidos básicos están la lisina, la arginina y la histidina. Tienen cadenas laterales que contienen nitrógeno y muestran basicidad. En especial, la lisina y la arginina suelen tener carga positiva, mientras que la histidina se considera una cadena lateral que puede protonarse según las condiciones. También son importantes al considerar el punto isoeléctrico de las proteínas y las interacciones con el ADN.
Aminoácidos aromáticos
Entre los aminoácidos aromáticos están la fenilalanina, la tirosina y el triptófano. Como poseen anillos aromáticos, forman un grupo fácil de distinguir incluso en la fórmula estructural. La tirosina tiene un -OH fenólico y el triptófano un anillo de indol. Los aminoácidos aromáticos también están relacionados con las interacciones hidrofóbicas en las proteínas y con la absorción de luz ultravioleta.
Aminoácidos con azufre
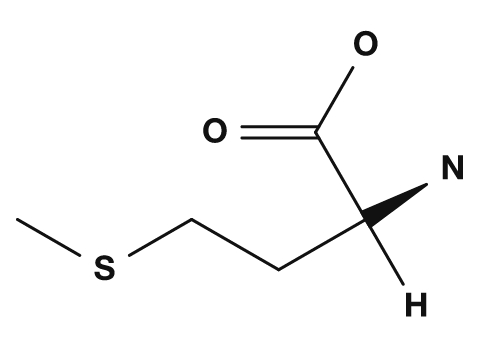
Entre los aminoácidos con azufre están la cisteína y la metionina. La cisteína posee un grupo tiol (-SH) y, cuando dos cisteínas se oxidan, pueden formar un enlace disulfuro. Este enlace es importante para estabilizar la estructura tridimensional de las proteínas. La metionina es un aminoácido con estructura de tioéter y se conoce también como el aminoácido representativo asociado al codón de inicio AUG, que corresponde al inicio de la traducción.
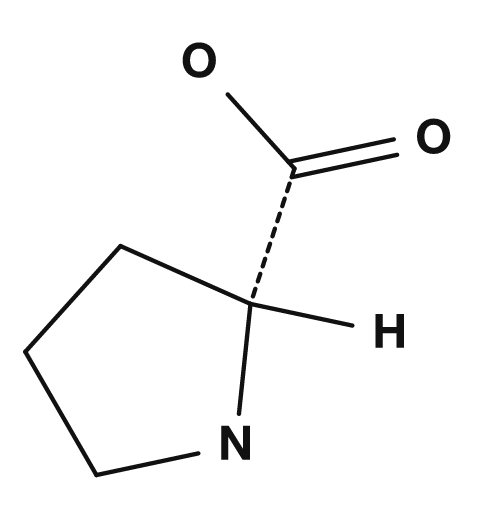
Prolina: una estructura especial
La prolina es un poco especial. En los aminoácidos habituales, el grupo amino es una amina primaria, pero en la prolina la cadena lateral vuelve al grupo amino formando un anillo, por lo que su estructura se aproxima a una amina secundaria. NCBI Bookshelf también explica que la prolina, a diferencia de otros aminoácidos, posee un grupo amino secundario. Por ello, la prolina está implicada en las curvas de la cadena principal de las proteínas y en restricciones estructurales.
Cómo leer las fórmulas estructurales
Al estudiar los 20 aminoácidos a través de fórmulas estructurales, es útil identificar primero el esqueleto común y luego comparar solo los grupos R. Comprobando los siguientes puntos del grupo R se pueden predecir las propiedades de un aminoácido.
- Mayoritariamente hidrocarburos → hidrofóbico
- Contiene oxígeno o nitrógeno → polar
- Tiene un grupo carboxilo adicional → ácido
- Tiene un grupo amino adicional → básico
- Tiene un anillo aromático → aromático
Resumen
Los 20 aminoácidos comparten el mismo esqueleto de alfa-aminoácido, pero sus propiedades cambian según las diferencias en la cadena lateral. Más que memorizar los nombres, organizarlos en categorías de no polares, polares, ácidos, básicos, aromáticos, con azufre y estructura especial facilita leer sus características a partir de las fórmulas estructurales.