Parmi les 20 acides aminés standard constituant les protéines, la glycine est particulière. La plupart des acides aminés possèdent un centre chiral et nécessitent la considération de stéréoisomères tels que les formes D et L. Cependant, seule la glycine n'a pas d'isomères optiques. La raison en est que la chaîne latérale de la glycine est un atome d'hydrogène.
Substituants au Carbone α : Glycine Versus Autres Acides Aminés
La structure générale d'un α-aminoacide peut s'exprimer comme suit :
H2N-CH(R)-COOH
Dans la plupart des acides aminés, le carbone α est lié à quatre substituants différents : un groupe amino, un groupe carboxyle, un atome d'hydrogène et un groupe R. Un tel carbone devient un centre chiral et possède des énantiomères.
Cependant, dans la glycine, le groupe R est l'hydrogène. Par conséquent, les substituants liés au carbone α sont : groupe amino, groupe carboxyle, hydrogène, hydrogène. Puisqu'il y a deux atomes d'hydrogène, les quatre substituants ne sont pas tous différents.
PubChem décrit la glycine comme l'acide aminé protéique le plus simple, avec un atome d'hydrogène comme chaîne latérale, et comme le seul acide aminé protéique achiral. NCBI Bookshelf explique également que les 20 acides aminés protéiques sont des L-isomères, avec des centres chiraux au carbone α sauf pour la glycine.
Comparaison de la Glycine et de l'Alanine
| Acide aminé | Substituants au carbone α | Centre chiral | Isomères optiques |
|---|---|---|---|
| Alanine (exemple) | NH2, COOH, H, CH3 |
Oui | Les formes D et L existent |
| Glycine | NH2, COOH, H, H |
Non | N'existent pas |
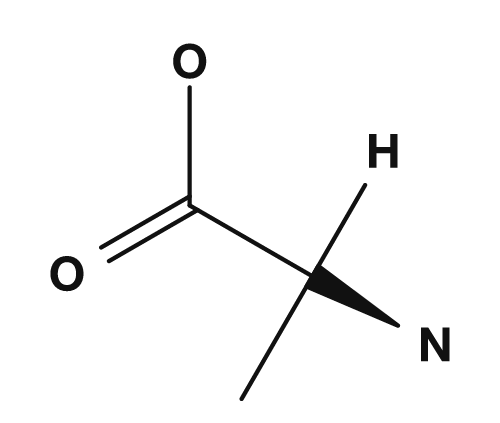
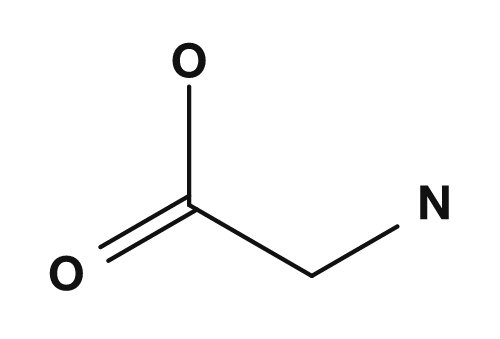
| Alanine | Glycine |
|---|---|
|
|
Centre Chiral et Isomères Optiques
Ne pas avoir de centre chiral signifie que la glycine n'a pas de distinction entre les formes D et L. Pour des acides aminés comme l'alanine et la valine, deux configurations qui sont des images spéculaires l'une de l'autre peuvent être distinguées, mais pour la glycine, puisqu'il y a deux substituants identiques autour du carbone α, l'image spéculaire peut être superposée à la structure originale. C'est pourquoi la glycine n'a pas d'isomères optiques.
Confirmation à Partir des Formules Structurales
Cette différence devient plus claire lorsqu'on la confirme avec des formules structurales.
- Alanine : carbone α lié à
NH2,COOH,H,CH3→ les quatre sont différents → chiral - Glycine : carbone α lié à
NH2,COOH,H,H→ deux hydrogènes → pas de centre chiral
En d'autres termes, la nature particulière de la glycine peut être comprise immédiatement à partir de la formule structurale.
Effet sur la Structure des Protéines
La petite taille de la glycine affecte également la structure des protéines. Parce que la chaîne latérale n'est que de l'hydrogène, la glycine a moins d'encombrement stérique que les autres acides aminés et tend à apparaître à des positions dans une protéine où la chaîne principale peut se déplacer relativement librement. Molecular Biology of the Cell de NCBI Bookshelf explique que la structure tridimensionnelle d'une protéine est déterminée par sa séquence d'acides aminés, et que les interactions entre chaînes latérales stabilisent le repliement. La petite chaîne latérale de la glycine joue un rôle unique dans de telles structures tridimensionnelles.
La glycine est également l'acide aminé le plus simple, ce qui la rend appropriée comme premier exemple lors de l'apprentissage de la structure de base des acides aminés. Cependant, dans les explications de chiralité, elle doit être traitée comme une exception. Il est important de comprendre que la plupart des acides aminés sont chiraux, mais que la glycine est différente.
Conditions pour un Centre Chiral
Comprendre la glycine aide également à comprendre naturellement les conditions pour un centre chiral.
- Le carbone a quatre liaisons (nécessaire mais pas suffisant)
- Les quatre substituants sont tous différents (c'est la condition nécessaire)
La glycine ne satisfait pas la condition 2, donc elle ne devient pas un centre chiral. Il ne suffit pas qu'un carbone ait simplement quatre liaisons. Les quatre substituants doivent tous être différents.
Résumé
La raison pour laquelle seule la glycine n'a pas d'isomères optiques est que sa chaîne latérale est un atome d'hydrogène et que le carbone α a deux atomes d'hydrogène identiques liés. Par conséquent, le carbone α n'a pas quatre substituants différents et ne devient pas un centre chiral. La glycine est le plus simple des acides aminés protéiques et le seul acide aminé achiral.