L'élément le plus important pour comprendre les acides aminés est la chaîne latérale. La chaîne latérale est également appelée groupe R et c'est la partie qui diffère entre les acides aminés. Bien que les acides aminés partagent un squelette commun, modifier le groupe R modifie des propriétés telles que la solubilité dans l'eau, la charge et la tendance à se trouver à l'intérieur d'une protéine. NCBI Bookshelf explique que les acides aminés possèdent un groupe α-carboxyle, un groupe α-amino et un groupe R, et que les différences entre les groupes R déterminent les propriétés uniques de chaque acide aminé.
La structure de base d'un acide aminé peut être représentée comme suit.
H2N-CH(R)-COOH
Bases de la chaîne latérale : exemples de groupes R
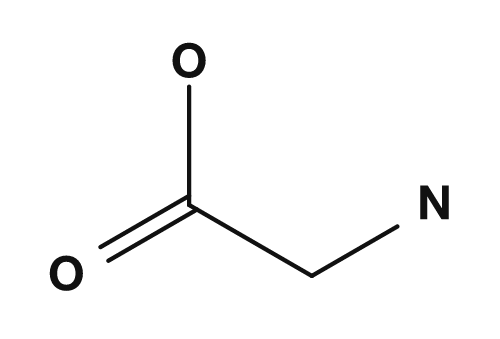
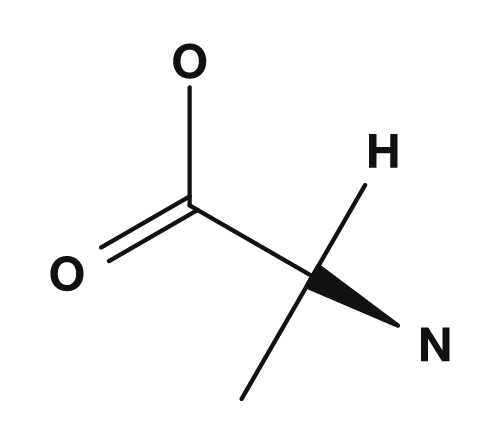
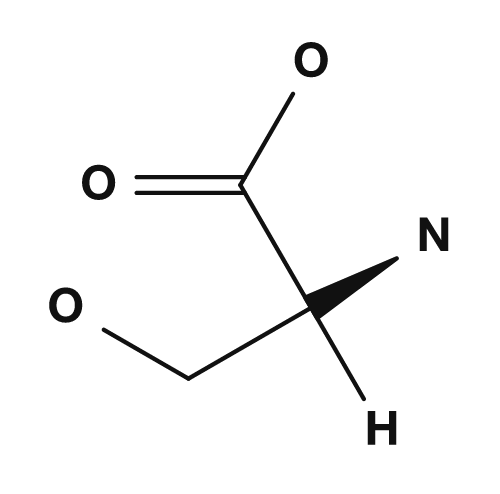
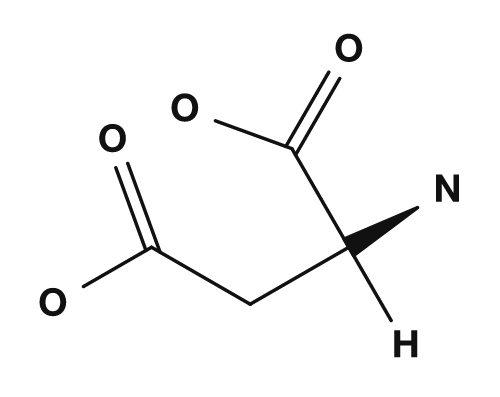
La partie R est la chaîne latérale. Par exemple, dans la glycine, le groupe R est un atome d'hydrogène, dans l'alanine c'est un groupe méthyle, dans la sérine c'est un groupe hydroxyméthyle et dans l'acide aspartique c'est un groupe carboxyméthyle. Ces petites différences ont un impact majeur sur les propriétés de l'acide aminé.
| Acide aminé | Groupe R | Caractéristiques |
|---|---|---|
| Glycine | Hydrogène | Plus petit acide aminé, achiral |
| Alanine | Groupe méthyle | Apolaire simple |
| Sérine | Groupe hydroxyméthyle | Polaire, participe aux liaisons hydrogène |
| Acide aspartique | Groupe carboxyméthyle | Acide, tend à porter une charge négative |
| Glycine | Alanine | Sérine | Acide aspartique |
|---|---|---|---|
|
|
|
|
Affinité avec l'eau : hydrophobe et hydrophile
La manière la plus fondamentale de classer les chaînes latérales est selon leur affinité avec l'eau.
- Les chaînes latérales contenant beaucoup d'hydrocarbures tendent à être hydrophobes et à se regrouper à l'intérieur de la protéine.
- Les chaînes latérales contenant de l'oxygène ou de l'azote tendent à participer aux liaisons hydrogène et sont donc hydrophiles.
La forme d'une protéine est largement influencée par ces interactions entre chaînes latérales. Molecular Biology of the Cell de NCBI Bookshelf explique que les acides aminés à chaînes latérales hydrophobes tendent à se rassembler à l'intérieur de la protéine et que les interactions non covalentes stabilisent la structure repliée.
Chaînes latérales acides et basiques
Le point important suivant concerne les chaînes latérales acides et basiques.
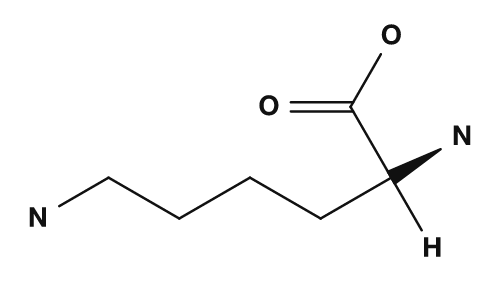
L'acide aspartique et l'acide glutamique possèdent des groupes carboxyle dans leur chaîne latérale et tendent à porter une charge négative au pH physiologique. La lysine, l'arginine et l'histidine contiennent un azote basique dans leur chaîne latérale. En particulier, la lysine et l'arginine tendent à porter une charge positive, et l'histidine est importante en tant que chaîne latérale facilement protonable selon les conditions. Un article publié dans PMC explique également qu'autour du pH neutre, l'acide aspartique et l'acide glutamique portent des charges négatives, et que la lysine, l'arginine et l'histidine sont traitées comme des acides aminés impliqués dans l'état de charge.
| Charge | Acides aminés représentatifs | Groupes fonctionnels de la chaîne latérale |
|---|---|---|
| Négative (acide) | Acide aspartique, acide glutamique | Groupe carboxyle |
| Positive (basique) | Lysine, arginine, histidine | Groupe amino, groupe guanidino, imidazole |
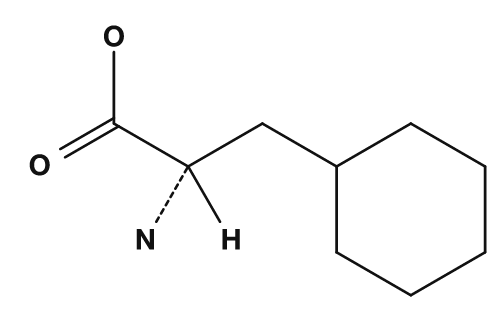
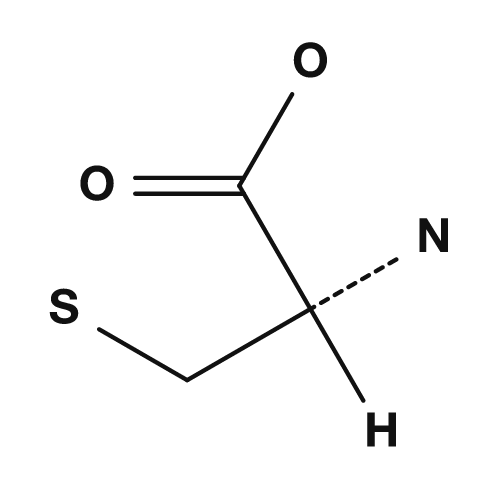
| Lysine | Phénylalanine | Cystéine |
|---|---|---|
|
|
|
Chaînes latérales aromatiques
Parmi les acides aminés à chaînes latérales aromatiques, on trouve la phénylalanine, la tyrosine et le tryptophane. Ils possèdent des systèmes d'électrons π cycliques et sont relativement faciles à repérer dans les formules structurales. La tyrosine a un groupe hydroxyle phénolique, ce qui lui confère des propriétés différentes de celles d'un simple aromatique hydrophobe. Le tryptophane a un grand cycle indole et est également important du point de vue de la structure des protéines et de l'absorption de la lumière.
Chaînes latérales contenant du soufre
Les chaînes latérales contenant du soufre méritent également l'attention.
La cystéine possède un groupe thiol (-SH), et lorsque deux cystéines sont oxydées, elles peuvent former un pont disulfure. Il s'agit d'une liaison importante qui stabilise la structure tridimensionnelle des protéines. La méthionine possède une structure de thioéther et est également bien connue comme l'acide aminé correspondant au codon d'initiation AUG pour l'initiation de la traduction.
| Type de chaîne latérale | Acides aminés représentatifs | Points clés |
|---|---|---|
| Hydrophobe | Valine, leucine, isoleucine | Tendent à se regrouper à l'intérieur des protéines |
| Aromatique | Phénylalanine, tyrosine, tryptophane | Système d'électrons π, impliqué dans l'absorption UV |
| Soufrée | Cystéine, méthionine | Ponts disulfures, lien avec le codon d'initiation AUG |
Comment lire les formules structurales
Lorsqu'on étudie les chaînes latérales, il est plus facile de comprendre en partant de la formule structurale plutôt qu'en mémorisant séparément les noms des acides aminés et leurs propriétés.
- Contient de l'oxygène ou de l'azote → tend à être polaire
- Contient un groupe carboxyle → tend à être acide
- Contient un groupe amino ou guanidino → tend à être basique
- Contient beaucoup d'hydrocarbures → tend à être hydrophobe
Résumé
La chaîne latérale d'un acide aminé est l'élément clé qui détermine ses propriétés. Les différences dans le groupe R donnent naissance à des caractéristiques telles que hydrophobie, hydrophilie, acidité, basicité, aromaticité et teneur en soufre. Lors de l'examen des formules structurales, prêter attention non seulement au squelette commun mais aussi à quels atomes et groupes fonctionnels sont présents dans la chaîne latérale facilite grandement la compréhension des propriétés des acides aminés.