Les acides aminés modifient leur état de charge en fonction du pH. En conditions acides, ils tendent à porter une charge positive, et en conditions basiques, une charge négative. Le point isoélectrique est essentiel pour comprendre ces variations de charge. Le point isoélectrique peut être compris comme le pH auquel la charge nette de la molécule devient nulle, avec un équilibre entre charges positives et négatives. L'IUPAC Gold Book décrit l'état isoélectrique comme l'état dans lequel un polyampholyte, notamment une protéine, ne présente pas d'électrophorèse.
pH et Variations de Charge
La structure de base des acides aminés comprend un groupe amino et un groupe carboxyle.
- En conditions acides, le groupe amino tend à accepter un proton pour devenir
-NH3+, tandis que le groupe carboxyle tend à prendre la forme-COOH. - En conditions basiques, le groupe carboxyle perd un proton pour devenir
-COO-, et le groupe amino s'approche de l'état-NH2. - À pH intermédiaire, la forme portant à la fois
-NH3+et-COO-(zwitterion) prédomine.
| Condition de pH | État du groupe amino | État du groupe carboxyle | Charge nette |
|---|---|---|---|
| Acide (pH bas) | -NH3+ (positif) |
-COOH (neutre) |
Positive |
| Proche du point isoélectrique | -NH3+ (positif) |
-COO- (négatif) |
0 (zwitterion) |
| Basique (pH élevé) | -NH2 (neutre) |
-COO- (négatif) |
Négative |
Qu'est-ce que le Point Isoélectrique ?
En prenant comme exemple la glycine, l'acide aminé le plus simple : du côté acide, elle tend à porter une charge globale positive, et du côté basique, une charge négative. Quelque part entre les deux se trouve un pH auquel la charge nette devient nulle. C'est le point isoélectrique de la glycine.
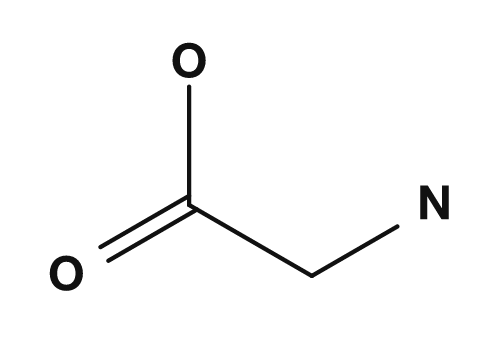
Pour comprendre le point isoélectrique, il est plus précis de le concevoir comme un état où les charges positives et négatives sont en équilibre, plutôt qu'un état sans charges. Les acides aminés tendent à exister sous forme de zwitterions près du pH neutre, portant simultanément des charges positives et négatives au sein de la molécule. PubChem explique que le zwitterion de la L-cystéinylglycine résulte du transfert d'un proton d'un groupe hydroxy vers un groupe amino, et constitue la principale microespèce à pH 7,3.
Comment les Chaînes Latérales Affectent le Point Isoélectrique
Le point isoélectrique varie selon le type de chaîne latérale.
- L'acide aspartique et l'acide glutamique, qui possèdent des groupes carboxyle dans leurs chaînes latérales, tendent à porter une charge négative, donc leurs points isoélectriques sont plus bas.
- Les acides aminés avec des chaînes latérales basiques, comme la lysine et l'arginine, tendent à porter une charge positive, donc leurs points isoélectriques sont plus élevés.
Un article de PMC explique que le pI d'une protéine est défini comme le pH auquel la charge nette est nulle, et dépend fortement de la composition en acides aminés et des valeurs de pKa de chaque chaîne latérale.
| Nature de la chaîne latérale | Acides aminés représentatifs | Effet sur le point isoélectrique |
|---|---|---|
| Chaîne latérale avec groupe carboxyle (acide) | Acide aspartique, Acide glutamique | Abaisse le point isoélectrique |
| Chaîne latérale avec azote basique (basique) | Lysine, Arginine, Histidine | Élève le point isoélectrique |
| Acide aspartique | Acide glutamique | Lysine |
|---|---|---|
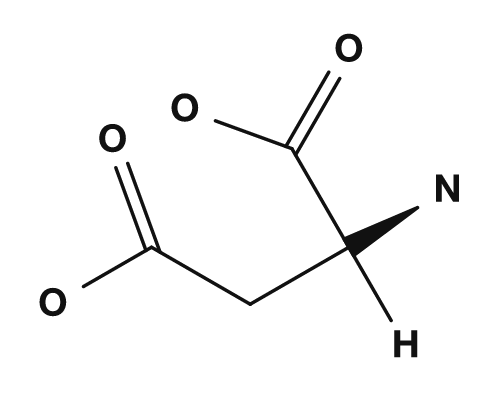
|
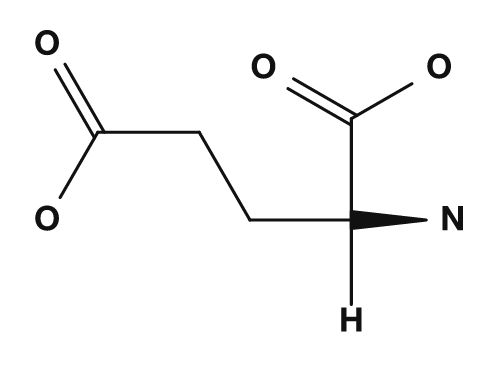
|
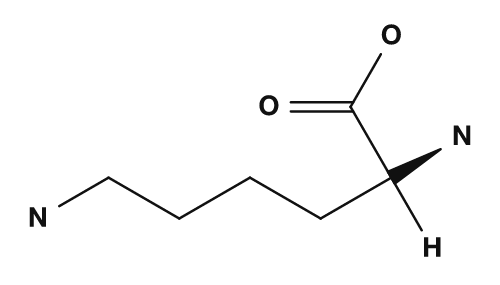
|
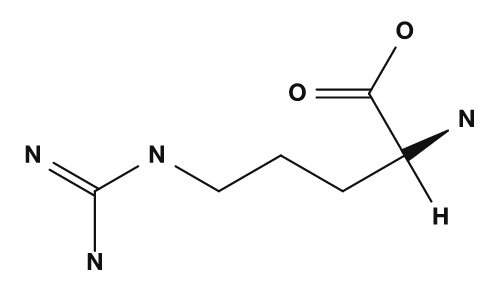
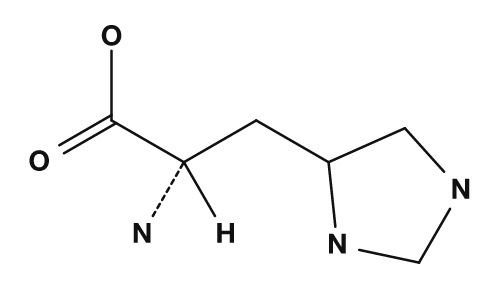
| Arginine | Histidine |
|---|---|
|
|
Réfléchir à la Charge à Partir des Formules Structurales
Lorsqu'on réfléchit au point isoélectrique à partir des formules structurales, la première étape consiste à rechercher les parties pouvant porter une charge.
- Identifier le groupe amino et le groupe carboxyle
- Vérifier si la chaîne latérale possède des groupes fonctionnels acides ou basiques
- Acide aspartique et acide glutamique → groupe carboxyle dans la chaîne latérale
- Lysine → groupe amino dans la chaîne latérale
- Arginine → groupe guanidino
- Histidine → cycle imidazole
Applications du Point Isoélectrique
Le point isoélectrique est également important dans la séparation et la purification des protéines. Puisque la charge nette d'une molécule change avec le pH, il est utilisé en électrophorèse et en chromatographie échangeuse d'ions.
- Lorsque le pH est inférieur au point isoélectrique → la molécule tend à être chargée positivement
- Lorsque le pH est supérieur au point isoélectrique → la molécule tend à être chargée négativement
Un article de PMC indique également que les protéines portent une charge positive à un pH inférieur au pI et une charge négative à un pH supérieur au pI.
Résumé
Le point isoélectrique est le pH auquel la charge nette d'un acide aminé ou d'une protéine devient nulle. Dans les acides aminés, les états d'ionisation du groupe amino, du groupe carboxyle et de la chaîne latérale changent avec le pH, de sorte que la charge change également. Lorsqu'on lit des formules structurales, chercher les groupes fonctionnels pouvant porter une charge est la première étape pour comprendre le point isoélectrique.