Les acides aminés représentatifs qui constituent les protéines sont au nombre de 20. Ils possèdent tous le même squelette de base, mais leur chaîne latérale (groupe R) diffère. NCBI Bookshelf cite comme les 20 acides aminés protéinogènes l'alanine, l'arginine, l'asparagine, l'acide aspartique, la cystéine, l'acide glutamique, la glutamine, la glycine, l'histidine, l'isoleucine, la leucine, la lysine, la méthionine, la phénylalanine, la proline, la sérine, la thréonine, le tryptophane, la tyrosine et la valine.
Pour mémoriser les 20 acides aminés, il est plus simple de les classer selon les propriétés de leur chaîne latérale plutôt que d'apprendre les noms par cœur.
Voici d'abord la liste des 20.
| Catégorie | Principaux acides aminés | Caractéristiques de la chaîne latérale |
|---|---|---|
| Apolaires | Glycine, alanine, valine, leucine, isoleucine, proline, méthionine | Se mélangent peu à l'eau |
| Polaires (non chargés) | Sérine, thréonine, asparagine, glutamine | Participent souvent à des liaisons hydrogène |
| Acides | Acide aspartique, acide glutamique | Charge négative au pH physiologique |
| Basiques | Lysine, arginine, histidine | Chaînes latérales basiques, susceptibles d'être chargées positivement |
| Aromatiques | Phénylalanine, tyrosine, tryptophane | Possèdent des cycles aromatiques |
| Soufrés | Cystéine, méthionine | Groupe thiol ou thioéther |
| Structure particulière | Proline | Amine secondaire, structure cyclique |
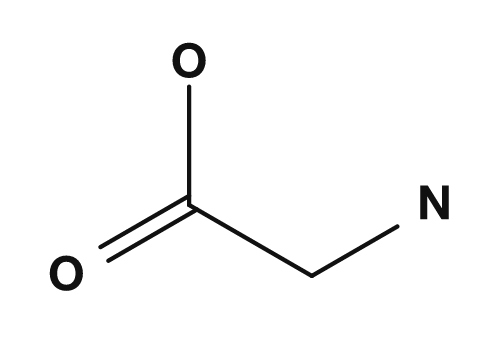
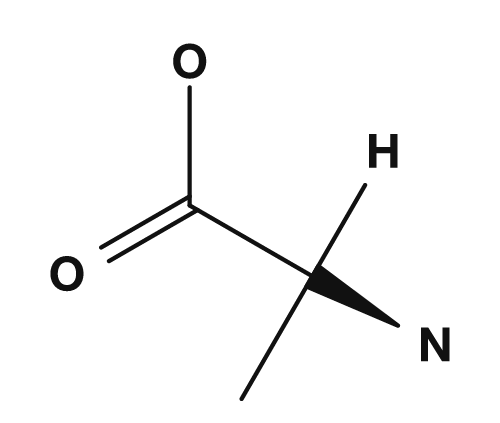
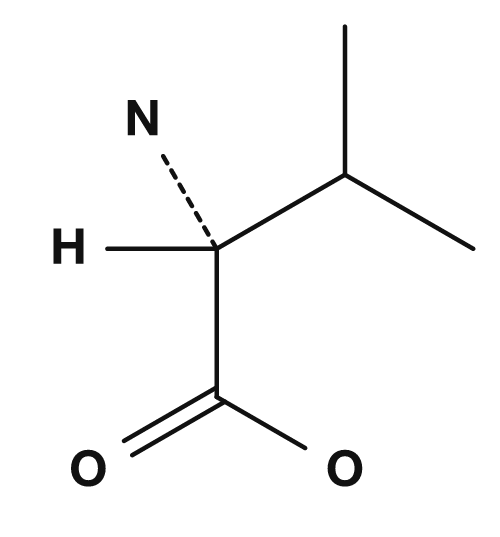
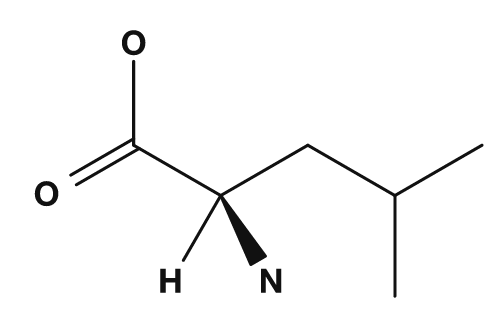
| Glycine | Alanine | Valine | Leucine | Isoleucine |
|---|---|---|---|---|
|
|
|
|
|
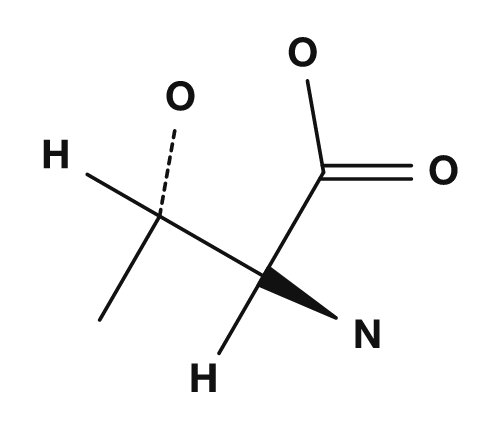
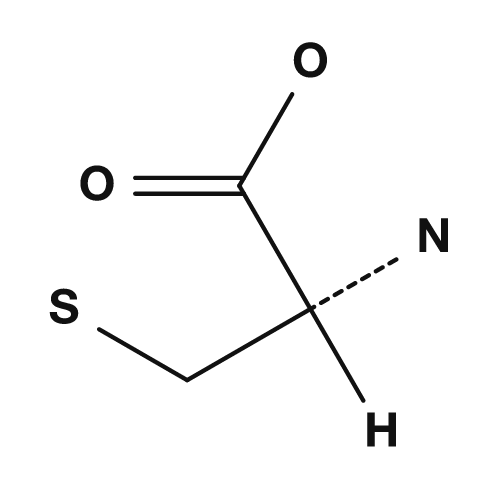
| Proline | Méthionine | Sérine | Thréonine | Cystéine |
|---|---|---|---|---|
|
|
|
|
|
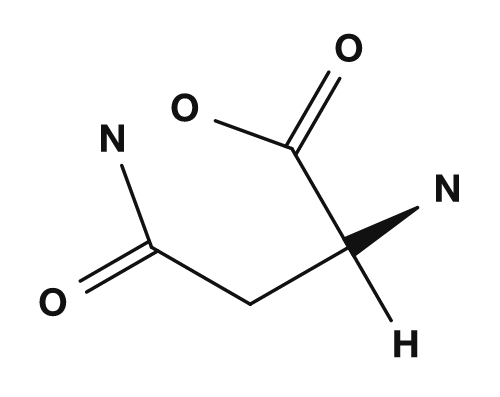
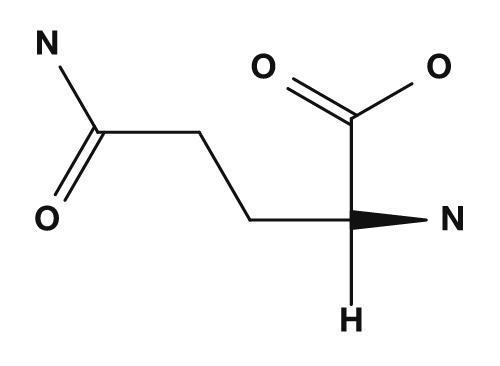
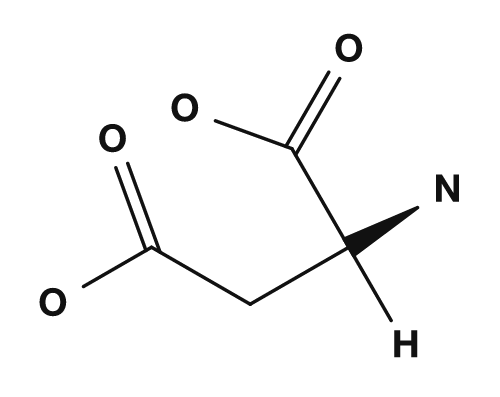
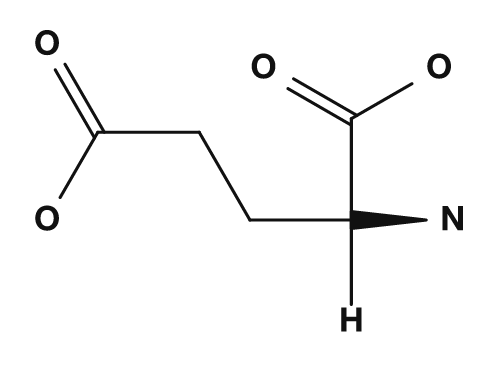
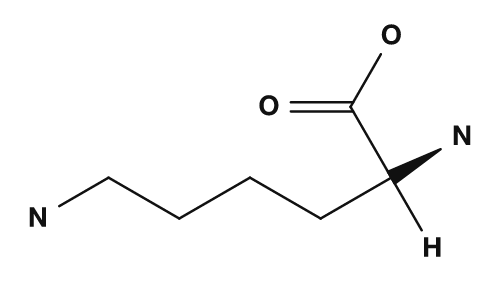
| Asparagine | Glutamine | Acide aspartique | Acide glutamique | Lysine |
|---|---|---|---|---|
|
|
|
|
|
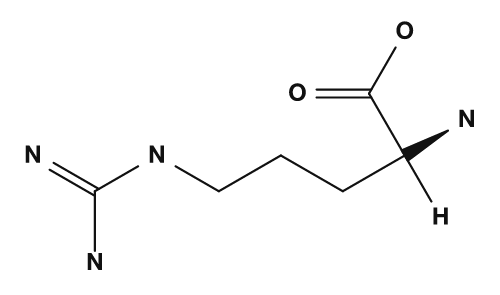
| Arginine | Histidine | Phénylalanine | Tyrosine | Tryptophane |
|---|---|---|---|---|
|
|
|
|
|
Acides aminés apolaires
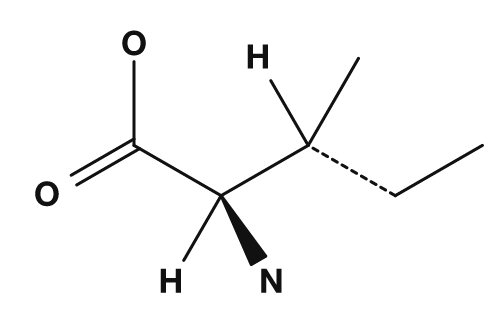
Parmi les acides aminés apolaires, on trouve la glycine, l'alanine, la valine, la leucine, l'isoleucine, la proline et la méthionine. Ils possèdent des chaînes latérales qui se mélangent mal à l'eau et ont tendance à se regrouper à l'intérieur des protéines. La valine, la leucine et l'isoleucine sont en particulier connues sous le nom d'acides aminés à chaîne ramifiée.
Acides aminés polaires (non chargés)
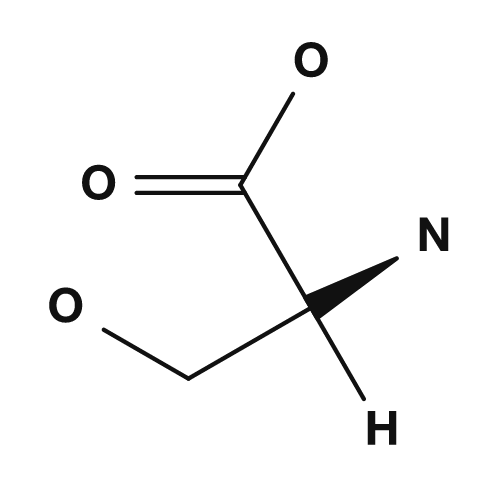
Parmi les acides aminés polaires mais peu enclins à porter une charge, on trouve la sérine, la thréonine, l'asparagine et la glutamine. Ils possèdent des chaînes latérales contenant de l'oxygène ou de l'azote et peuvent participer à des liaisons hydrogène. Ils interagissent avec l'eau à la surface des protéines et jouent un rôle important dans les sites actifs des enzymes.
Acides aminés acides et basiques
Acides aminés acides
Les acides aminés acides sont l'acide aspartique et l'acide glutamique. Ils possèdent un groupe carboxyle dans leur chaîne latérale et portent fréquemment une charge négative au pH physiologique.
Acides aminés basiques
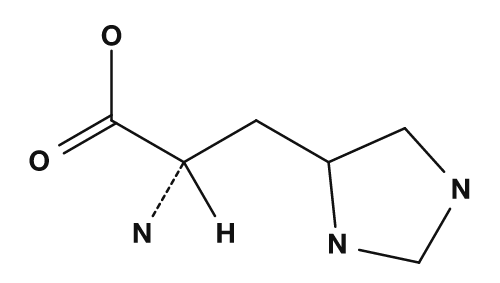
Les acides aminés basiques sont la lysine, l'arginine et l'histidine. Ils possèdent des chaînes latérales contenant de l'azote et présentent un caractère basique. La lysine et l'arginine portent souvent une charge positive, tandis que l'histidine est considérée comme une chaîne latérale facilement protonable selon les conditions. Ils sont également importants pour considérer le point isoélectrique des protéines et leurs interactions avec l'ADN.
Acides aminés aromatiques
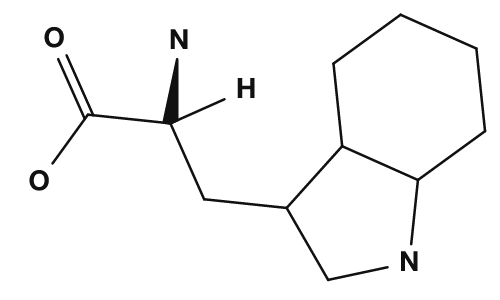
Les acides aminés aromatiques sont la phénylalanine, la tyrosine et le tryptophane. Comme ils possèdent des cycles aromatiques, ils forment un groupe facile à reconnaître sur une formule développée. La tyrosine porte un -OH phénolique et le tryptophane un cycle indole. Les acides aminés aromatiques interviennent aussi dans les interactions hydrophobes au sein des protéines et dans l'absorption ultraviolette.
Acides aminés soufrés
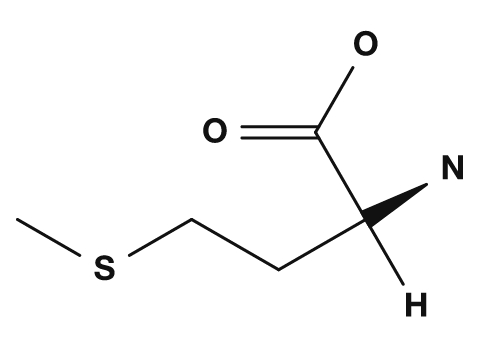
Les acides aminés soufrés sont la cystéine et la méthionine. La cystéine possède un groupe thiol (-SH), et lorsque deux cystéines sont oxydées, elles peuvent former un pont disulfure. Cette liaison est importante pour stabiliser la structure tridimensionnelle des protéines. La méthionine est un acide aminé à structure thioéther, également connu comme l'acide aminé associé au codon d'initiation AUG correspondant au démarrage de la traduction.
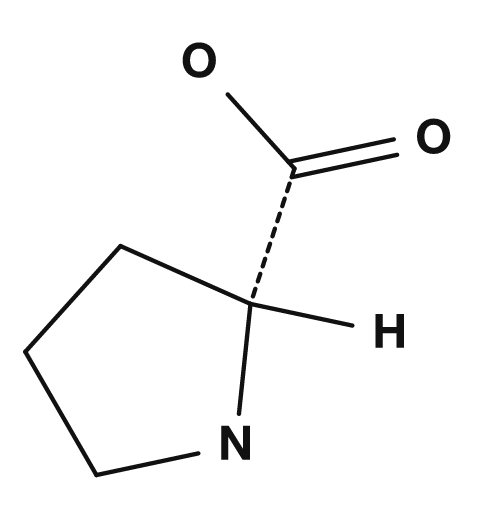
La proline : une structure particulière
La proline est quelque peu particulière. Dans la plupart des acides aminés, le groupe amine est une amine primaire, mais chez la proline la chaîne latérale revient sur le groupe amine pour former un cycle, ce qui lui confère une structure proche d'une amine secondaire. NCBI Bookshelf indique également que la proline, contrairement aux autres acides aminés, possède un groupe amino secondaire. Pour cette raison, la proline est associée aux courbures de la chaîne principale des protéines et à des contraintes structurales.
Comment lire les formules développées
Lors de l'étude des 20 acides aminés à partir de formules développées, il est utile de repérer d'abord le squelette commun, puis de comparer uniquement les groupes R. En vérifiant les points suivants concernant le groupe R, on peut prédire les propriétés d'un acide aminé.
- Principalement des hydrocarbures → hydrophobe
- Contient de l'oxygène ou de l'azote → polaire
- Possède un groupe carboxyle supplémentaire → acide
- Possède un groupe amine supplémentaire → basique
- Possède un cycle aromatique → aromatique
Résumé
Les 20 acides aminés partagent le même squelette d'acide α-aminé, mais leurs propriétés varient selon les différences au niveau de la chaîne latérale. Plutôt que de retenir uniquement les noms, les organiser dans les catégories apolaires, polaires, acides, basiques, aromatiques, soufrés et à structure particulière facilite la lecture des caractéristiques à partir des formules développées.