Unter den 20 Standardaminosäuren, aus denen Proteine aufgebaut sind, ist Glycin etwas Besonderes. Die meisten Aminosäuren besitzen ein chirales Zentrum und erfordern die Betrachtung von Stereoisomeren wie D- und L-Formen. Aber nur Glycin hat keine optischen Isomere. Der Grund dafür ist, dass Glycins Seitenkette ein Wasserstoffatom ist.
Substituenten am α-Kohlenstoff: Glycin Versus Andere Aminosäuren
Die allgemeine Struktur einer α-Aminosäure lässt sich wie folgt ausdrücken:
H2N-CH(R)-COOH
Bei den meisten Aminosäuren ist das α-Kohlenstoffatom an vier verschiedene Substituenten gebunden: eine Aminogruppe, eine Carboxylgruppe, ein Wasserstoffatom und eine R-Gruppe. Ein solches Kohlenstoffatom wird zu einem chiralen Zentrum und besitzt Enantiomere.
Bei Glycin ist die R-Gruppe jedoch Wasserstoff. Daher sind die am α-Kohlenstoff gebundenen Substituenten: Aminogruppe, Carboxylgruppe, Wasserstoff, Wasserstoff. Da zwei Wasserstoffatome vorhanden sind, sind nicht alle vier Substituenten verschieden.
PubChem beschreibt Glycin als die einfachste proteinbildende Aminosäure mit einem Wasserstoffatom als Seitenkette und als die einzige achirale proteinbildende Aminosäure. NCBI Bookshelf erklärt auch, dass alle 20 proteinbildenden Aminosäuren L-Isomere sind, mit chiralen Zentren am α-Kohlenstoff außer bei Glycin.
Vergleich von Glycin und Alanin
| Aminosäure | Substituenten am α-Kohlenstoff | Chirales Zentrum | Optische Isomere |
|---|---|---|---|
| Alanin (Beispiel) | NH2, COOH, H, CH3 |
Ja | D- und L-Formen existieren |
| Glycin | NH2, COOH, H, H |
Nein | Existieren nicht |
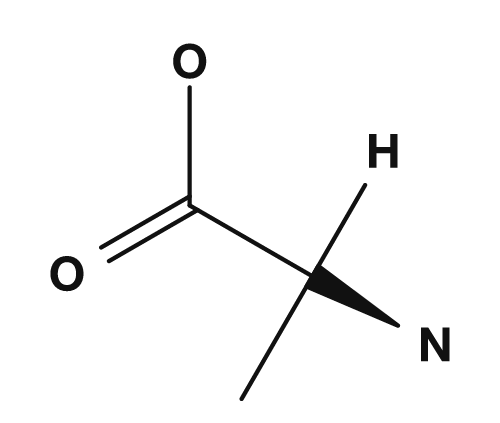
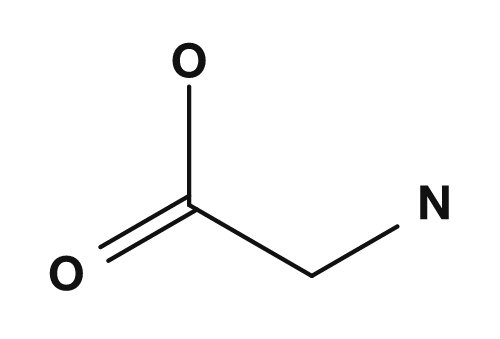
| Alanin | Glycin |
|---|---|
|
|
Chirales Zentrum und Optische Isomere
Kein chirales Zentrum zu haben bedeutet, dass Glycin keine Unterscheidung zwischen D- und L-Formen hat. Bei Aminosäuren wie Alanin und Valin können zwei Konfigurationen, die Spiegelbilder voneinander sind, unterschieden werden, aber bei Glycin können, da um das α-Kohlenstoffatom zwei identische Substituenten vorhanden sind, das Spiegelbild und die ursprüngliche Struktur zur Deckung gebracht werden. Deshalb hat Glycin keine optischen Isomere.
Bestätigung aus Strukturformeln
Dieser Unterschied wird bei der Bestätigung mit Strukturformeln deutlicher.
- Alanin: α-Kohlenstoff gebunden an
NH2,COOH,H,CH3→ alle vier sind verschieden → chiral - Glycin: α-Kohlenstoff gebunden an
NH2,COOH,H,H→ zwei Wasserstoffe → kein chirales Zentrum
Mit anderen Worten, Glycins besondere Natur kann sofort aus der Strukturformel verstanden werden.
Auswirkung auf die Proteinstruktur
Die geringe Größe von Glycin beeinflusst auch die Proteinstruktur. Da die Seitenkette nur Wasserstoff ist, hat Glycin weniger sterische Hinderung als andere Aminosäuren und neigt dazu, an Positionen in einem Protein aufzutreten, wo sich das Hauptgerüst relativ frei bewegen kann. NCBI Bookshelf's Molecular Biology of the Cell erklärt, dass die dreidimensionale Struktur eines Proteins durch seine Aminosäuresequenz bestimmt wird, und dass Wechselwirkungen zwischen Seitenketten die Faltung stabilisieren. Glycins kleine Seitenkette spielt eine einzigartige Rolle in solchen dreidimensionalen Strukturen.
Glycin ist auch die einfachste Aminosäure, was es zu dem ersten Beispiel beim Lernen über die Grundstruktur von Aminosäuren geeignet macht. Bei der Erklärung der Chiralität muss es jedoch als Ausnahme behandelt werden. Es ist wichtig zu verstehen, dass die meisten Aminosäuren chiral sind, aber Glycin ist anders.
Bedingungen für ein Chirales Zentrum
Das Verständnis von Glycin hilft einem auch, die Bedingungen für ein chirales Zentrum natürlich zu verstehen.
- Das Kohlenstoffatom hat vier Bindungen (notwendig, aber nicht hinreichend)
- Die vier Substituenten sind alle verschieden (dies ist die notwendige Bedingung)
Glycin erfüllt Bedingung 2 nicht, daher wird es kein chirales Zentrum. Es reicht nicht aus, dass ein Kohlenstoffatom einfach vier Bindungen hat. Alle vier Substituenten müssen verschieden sein.
Zusammenfassung
Der Grund, warum nur Glycin keine optischen Isomere hat, ist, dass seine Seitenkette ein Wasserstoffatom ist und das α-Kohlenstoffatom zwei identische Wasserstoffatome gebunden hat. Daher hat das α-Kohlenstoffatom nicht vier verschiedene Substituenten und wird kein chirales Zentrum. Glycin ist die einfachste der proteinbildenden Aminosäuren und die einzige achirale Aminosäure.