Die meisten Aminosäuren besitzen Stereoisomere. Der Grund dafür ist, dass das α-Kohlenstoffatom ein chirales Zentrum darstellt. Ein chirales Zentrum ist ein Kohlenstoffatom, das mit vier verschiedenen Substituenten verbunden ist. Bei den meisten proteinbildenden α-Aminosäuren ist das α-Kohlenstoffatom an eine Aminogruppe, eine Carboxylgruppe, ein Wasserstoffatom und eine Seitenkette R gebunden, was es zu einem chiralen Zentrum macht. NCBI Bookshelf erklärt, dass proteinbildende Aminosäuren α-Aminosäuren sind und alle außer Glycin ein chirales Zentrum am α-Kohlenstoff haben.
D- und L-Notation
Eine gängige Notation in der Stereochemie der Aminosäuren sind D-Form und L-Form. Die D/L-Notation stellt die relative Konfiguration auf Basis von Glycerinaldehyd als Referenz dar. Die Standardaminosäuren, aus denen Proteine aufgebaut sind, sind grundsätzlich L-Aminosäuren. NCBI Bookshelf gibt auch an, dass alle 20 Aminosäuren in Proteinen das L-Isomer sind.
Unterschied Zwischen D/L-Notation und R/S-Notation
D/L-Notation und R/S-Notation sind nicht dasselbe.
| Notationssystem | Basis | Proteinbildende Aminosäuren | Ausnahmen |
|---|---|---|---|
| D/L-Notation | Relative Konfiguration auf Basis von Glycerinaldehyd | L-Form | Glycin (kein chirales Zentrum) |
| R/S-Notation | Absolute Konfiguration nach CIP-Prioritätsregeln | Überwiegend S-Konfiguration | Cystein (R-Konfiguration) |
D/L ist eine Notation basierend auf der historischen relativen Konfiguration, während R/S eine absolute Konfiguration nach CIP-Prioritätsregeln ist. Die meisten L-Aminosäuren haben die S-Konfiguration, aber Cystein ist eine Ausnahme — seine Seitenkette enthält Schwefel, was die Prioritätsreihenfolge ändert und ihm die R-Konfiguration verleiht. NCBI Bookshelf gibt auch an, dass Standardaminosäuren außer Glycin und Cystein in der R/S-Notation die S-Konfiguration haben, während Cystein aufgrund seiner schwefelhaltigen R-Gruppe die R-Konfiguration hat.
Identifizierung Chiraler Zentren aus Strukturformeln
Wenn man in einer Strukturformel nach einem chiralen Zentrum sucht, konzentriert man sich auf das α-Kohlenstoffatom. Wenn die vier an diesem Kohlenstoff gebundenen Substituenten alle unterschiedlich sind, handelt es sich um ein chirales Zentrum.
| Aminosäure | Substituenten am α-Kohlenstoff | Chirales Zentrum |
|---|---|---|
| Alanin | NH2, COOH, H, CH3 |
Ja (alle vier sind unterschiedlich) |
| Glycin | NH2, COOH, H, H |
Nein (zwei Wasserstoffe) |
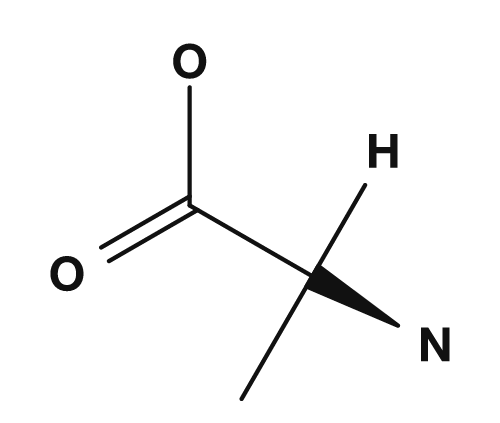
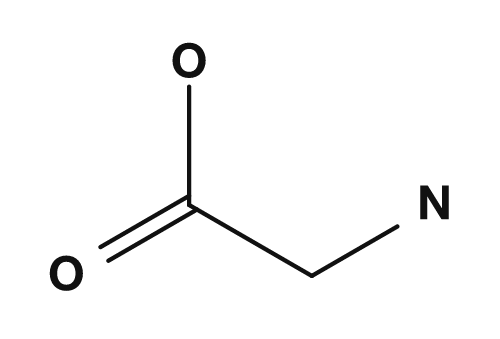
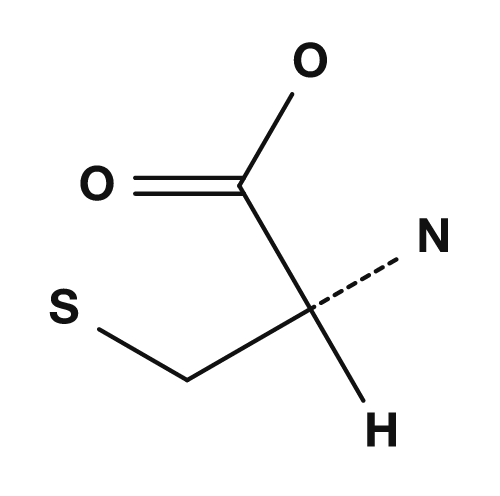
| Alanin | Glycin | Cystein |
|---|---|---|
|
|
|
Bei Alanin ist das α-Kohlenstoffatom an NH2, COOH, H und CH3 gebunden. Da alle vier unterschiedlich sind, ist Alanin chiral. Bei Glycin ist die R-Gruppe Wasserstoff, daher ist das α-Kohlenstoffatom an NH2, COOH, H und H gebunden — es gibt nur drei verschiedene Substituenten, daher hat es kein chirales Zentrum. PubChem gibt auch an, dass Glycin mit einem Wasserstoffatom als Seitenkette die einzige achirale proteinbildende Aminosäure ist.
D- und L-Formen und Optische Drehung
D-Form und L-Form stehen als Enantiomere (Spiegelbilder) in Beziehung zueinander. Wenn zwei Moleküle mit gleicher Molekülformel und gleichen Bindungsbeziehungen nicht auf ihr Spiegelbild überlagert werden können, werden sie als Enantiomere bezeichnet. Bei Aminosäuren beeinflusst dieser Unterschied in der räumlichen Konfiguration stark die Wechselwirkungen mit biologischen Molekülen. Da Enzyme und Rezeptoren in lebenden Organismen dreidimensionale Strukturen haben, können sie zwischen L- und D-Formen unterscheiden.
Ein wichtiger Punkt beim Erlernen der D/L-Notation für Aminosäuren ist, nicht einfach zu denken, dass „L linksdrehend" oder „D rechtsdrehend" bedeutet. Die D/L-Notation gibt nicht direkt die Richtung der optischen Drehung an. Die optische Drehung ist eine experimentell gemessene Eigenschaft, die als + oder - ausgedrückt wird. D/L ist ein Symbol für die strukturelle relative Konfiguration.
Schlüsselpunkte für das Lernen aus Strukturformeln
Beim Lernen aus Strukturformeln ist der erste Schritt zu überprüfen, ob das α-Kohlenstoffatom vier verschiedene Substituenten hat.
- Überprüfen, ob das α-Kohlenstoffatom vier verschiedene Substituenten hat
- Glycin hat ausnahmsweise kein chirales Zentrum
- Aminosäuren in Proteinen sind grundsätzlich L-Form
- D/L-Notation und R/S-Notation sind verschiedene Systeme
- Cystein ist eine Ausnahme: L-Form, aber R-Konfiguration
Zusammenfassung
Die meisten Aminosäuren sind chiral, weil das α-Kohlenstoffatom vier verschiedene Substituenten hat. Die Standardaminosäuren in Proteinen sind grundsätzlich L-Form, und nur Glycin fehlt ein chirales Zentrum, weil es zwei identische Wasserstoffatome am α-Kohlenstoff hat. D/L-Notation und R/S-Notation sind verschiedene Systeme, und Cystein muss insbesondere als Ausnahme verstanden werden.