Aminosäuren ändern ihren Ladungszustand in Abhängigkeit vom pH-Wert. Unter sauren Bedingungen neigen sie dazu, eine positive Ladung zu tragen, unter basischen Bedingungen eine negative. Der isoelektrische Punkt ist entscheidend für das Verständnis dieser Ladungsänderungen. Der isoelektrische Punkt kann als der pH-Wert verstanden werden, bei dem die Nettoladung des Moleküls null wird, wobei positive und negative Ladungen im Gleichgewicht stehen. Das IUPAC Gold Book beschreibt den isoelektrischen Zustand als den Zustand, in dem ein Polyampholyt, insbesondere ein Protein, keine Elektrophorese zeigt.
pH-Wert und Ladungsänderungen
Die Grundstruktur von Aminosäuren enthält eine Aminogruppe und eine Carboxylgruppe.
- Unter sauren Bedingungen neigt die Aminogruppe dazu, ein Proton aufzunehmen und
-NH3+zu werden, während die Carboxylgruppe die Form-COOHannimmt. - Unter basischen Bedingungen verliert die Carboxylgruppe ein Proton und wird
-COO-, und die Aminogruppe nähert sich dem-NH2-Zustand. - Bei mittlerem pH überwiegt die Form mit sowohl
-NH3+als auch-COO-(Zwitterion).
| pH-Bedingung | Zustand der Aminogruppe | Zustand der Carboxylgruppe | Nettoladung |
|---|---|---|---|
| Sauer (niedriger pH) | -NH3+ (positiv) |
-COOH (neutral) |
Positiv |
| In der Nähe des isoelektrischen Punkts | -NH3+ (positiv) |
-COO- (negativ) |
0 (Zwitterion) |
| Basisch (hoher pH) | -NH2 (neutral) |
-COO- (negativ) |
Negativ |
Was Ist der Isoelektrische Punkt?
Am Beispiel von Glycin, der einfachsten Aminosäure: Auf der sauren Seite neigt es dazu, insgesamt eine positive Ladung zu tragen, und auf der basischen Seite eine negative Ladung. Irgendwo dazwischen liegt ein pH-Wert, bei dem die Nettoladung null wird. Das ist der isoelektrische Punkt von Glycin.
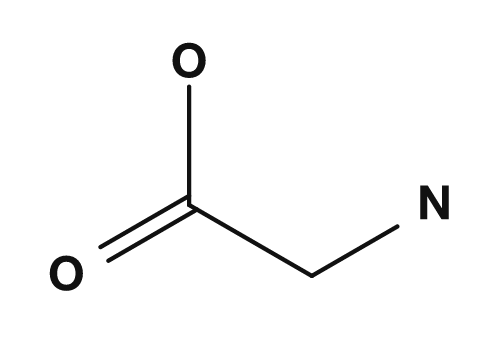
Beim Verständnis des isoelektrischen Punkts ist es genauer, ihn als einen Zustand zu betrachten, in dem positive und negative Ladungen im Gleichgewicht sind, anstatt als einen Zustand ohne Ladungen. Aminosäuren existieren in der Nähe des neutralen pH als Zwitterionen, die sowohl positive als auch negative Ladungen im Molekül tragen. PubChem erklärt, dass das Zwitterion von L-Cysteinylglycin durch den Transfer eines Protons von einer Hydroxygruppe zu einer Aminogruppe entsteht und bei pH 7,3 die dominante Mikrospezies ist.
Wie Seitenketten den Isoelektrischen Punkt Beeinflussen
Der isoelektrische Punkt variiert je nach Art der Seitenkette.
- Asparaginsäure und Glutaminsäure, die Carboxylgruppen in ihren Seitenketten haben, neigen dazu, eine negative Ladung zu tragen, daher sind ihre isoelektrischen Punkte niedriger.
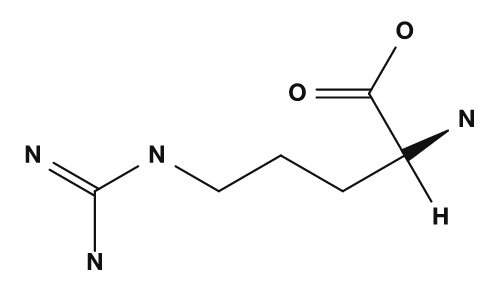
- Aminosäuren mit basischen Seitenketten, wie Lysin und Arginin, neigen dazu, eine positive Ladung zu tragen, daher sind ihre isoelektrischen Punkte höher.
Ein PMC-Artikel erklärt, dass der pI eines Proteins als der pH-Wert definiert ist, bei dem die Nettoladung null ist, und stark von der Aminosäurezusammensetzung und den pKa-Werten der einzelnen Seitenketten abhängt.
| Seitenkettennatur | Repräsentative Aminosäuren | Auswirkung auf den isoelektrischen Punkt |
|---|---|---|
| Seitenkette mit Carboxylgruppe (sauer) | Asparaginsäure, Glutaminsäure | Senkt den isoelektrischen Punkt |
| Seitenkette mit basischem Stickstoff (basisch) | Lysin, Arginin, Histidin | Erhöht den isoelektrischen Punkt |
| Asparaginsäure | Glutaminsäure | Lysin |
|---|---|---|
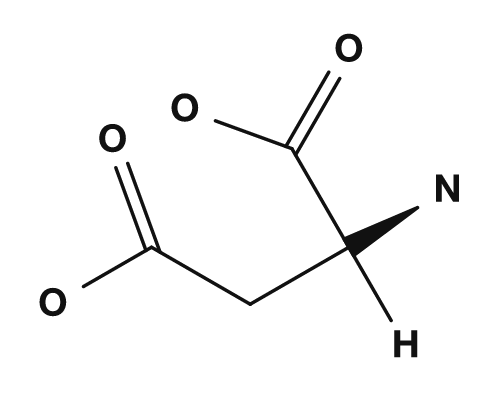
|
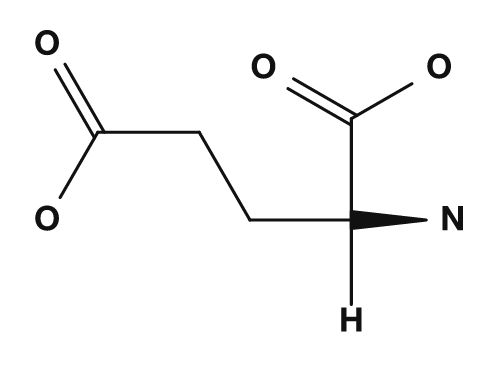
|
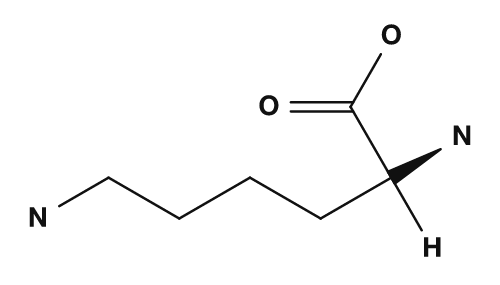
|
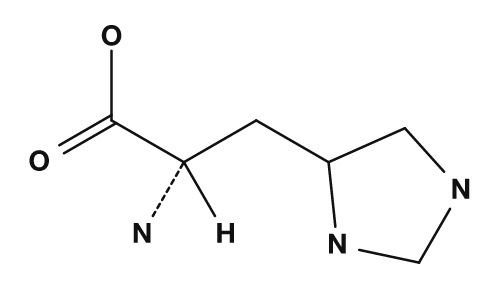
| Arginin | Histidin |
|---|---|
|
|
Über Ladung aus Strukturformeln Nachdenken
Wenn man den isoelektrischen Punkt aus Strukturformeln betrachtet, ist der erste Schritt, nach Teilen zu suchen, die eine Ladung tragen können.
- Die Aminogruppe und die Carboxylgruppe identifizieren
- Prüfen, ob die Seitenkette saure oder basische funktionelle Gruppen hat
- Asparaginsäure und Glutaminsäure → Carboxylgruppe in der Seitenkette
- Lysin → Aminogruppe in der Seitenkette
- Arginin → Guanidinogruppe
- Histidin → Imidazolring
Anwendungen des Isoelektrischen Punkts
Der isoelektrische Punkt ist auch bei der Trennung und Reinigung von Proteinen wichtig. Da sich die Nettoladung eines Moleküls mit dem pH-Wert ändert, wird er in der Elektrophorese und der Ionenaustauschchromatographie eingesetzt.
- Wenn der pH-Wert unter dem isoelektrischen Punkt liegt → das Molekül ist tendenziell positiv geladen
- Wenn der pH-Wert über dem isoelektrischen Punkt liegt → das Molekül ist tendenziell negativ geladen
Ein PMC-Artikel besagt auch, dass Proteine bei einem pH-Wert unterhalb des pI eine positive Ladung und oberhalb eine negative Ladung tragen.
Zusammenfassung
Der isoelektrische Punkt ist der pH-Wert, bei dem die Nettoladung einer Aminosäure oder eines Proteins null wird. Bei Aminosäuren ändern sich die Ionisierungszustände der Aminogruppe, der Carboxylgruppe und der Seitenkette mit dem pH-Wert, sodass sich auch die Ladung ändert. Wenn man Strukturformeln liest, ist die Suche nach funktionellen Gruppen, die eine Ladung tragen können, der erste Schritt zum Verständnis des isoelektrischen Punkts.