Der wichtigste Bestandteil zum Verständnis von Aminosäuren ist die Seitenkette. Die Seitenkette wird auch als R-Gruppe bezeichnet und ist der Teil, der sich zwischen den Aminosäuren unterscheidet. Aminosäuren haben zwar ein gemeinsames Grundgerüst, aber die Veränderung der R-Gruppe verändert Eigenschaften wie Wasserlöslichkeit, Ladung und die Tendenz, im Inneren eines Proteins zu liegen. NCBI Bookshelf erklärt, dass Aminosäuren eine α-Carboxylgruppe, eine α-Aminogruppe und eine R-Gruppe besitzen und dass Unterschiede in der R-Gruppe die einzigartigen Eigenschaften jeder Aminosäure bestimmen.
Die Grundstruktur einer Aminosäure kann wie folgt dargestellt werden.
H2N-CH(R)-COOH
Grundlagen der Seitenkette: Beispiele für R-Gruppen
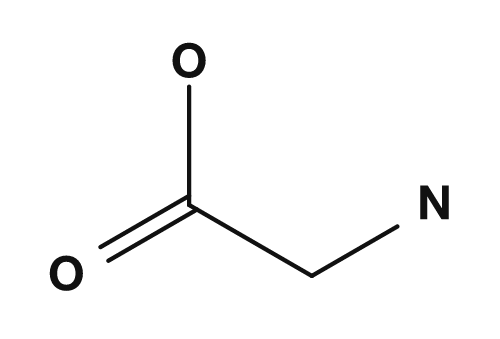
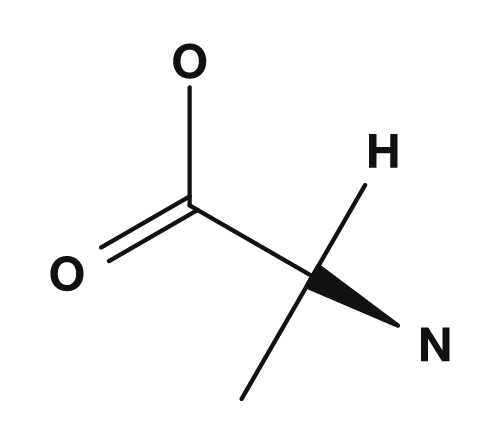
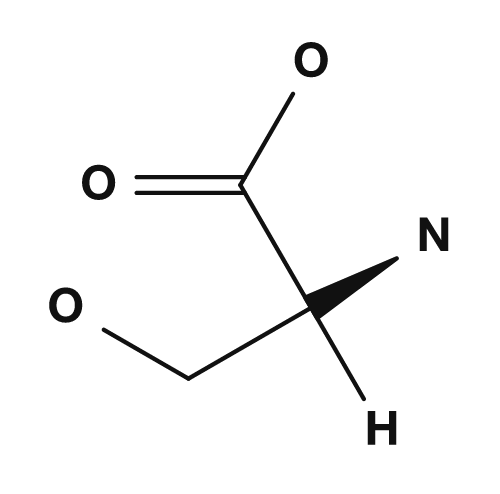
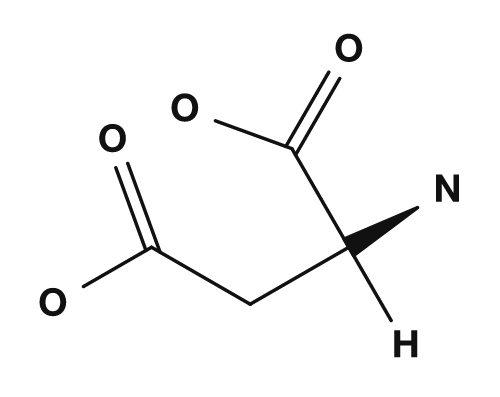
Der R-Teil ist die Seitenkette. Bei Glycin ist die R-Gruppe beispielsweise ein Wasserstoffatom, bei Alanin eine Methylgruppe, bei Serin eine Hydroxymethylgruppe und bei Asparaginsäure eine Carboxymethylgruppe. Diese kleinen Unterschiede haben einen großen Einfluss auf die Eigenschaften der Aminosäure.
| Aminosäure | R-Gruppe | Merkmale |
|---|---|---|
| Glycin | Wasserstoff | Kleinste Aminosäure, achiral |
| Alanin | Methylgruppe | Einfach unpolar |
| Serin | Hydroxymethylgruppe | Polar, an Wasserstoffbrücken beteiligt |
| Asparaginsäure | Carboxymethylgruppe | Sauer, trägt häufig eine negative Ladung |
| Glycin | Alanin | Serin | Asparaginsäure |
|---|---|---|---|
|
|
|
|
Affinität zu Wasser: hydrophob und hydrophil
Die grundlegendste Möglichkeit, Seitenketten zu klassifizieren, ist ihre Affinität zu Wasser.
- Seitenketten, die viele Kohlenwasserstoffe enthalten, neigen dazu, hydrophob zu sein und sich im Inneren des Proteins zu sammeln.
- Seitenketten, die Sauerstoff oder Stickstoff enthalten, neigen dazu, an Wasserstoffbrücken teilzunehmen, und sind daher hydrophil.
Die Form eines Proteins wird stark durch solche Wechselwirkungen zwischen Seitenketten beeinflusst. Molecular Biology of the Cell von NCBI Bookshelf erklärt, dass Aminosäuren mit hydrophoben Seitenketten dazu neigen, sich im Inneren des Proteins anzusammeln, und dass nichtkovalente Wechselwirkungen die Faltungsstruktur stabilisieren.
Saure und basische Seitenketten
Der nächste wichtige Punkt sind saure und basische Seitenketten.
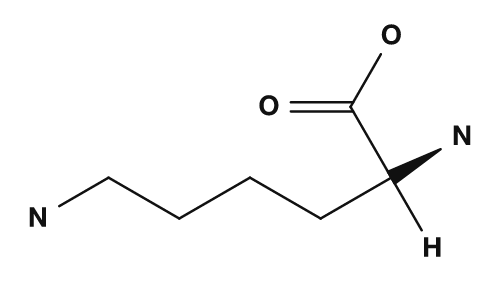
Asparaginsäure und Glutaminsäure haben Carboxylgruppen in ihrer Seitenkette und tragen bei physiologischem pH-Wert tendenziell eine negative Ladung. Lysin, Arginin und Histidin enthalten basischen Stickstoff in ihrer Seitenkette. Insbesondere Lysin und Arginin neigen dazu, eine positive Ladung zu tragen, und Histidin ist als Seitenkette wichtig, die je nach Bedingungen leicht protoniert werden kann. Auch eine in PMC veröffentlichte Arbeit erklärt, dass im neutralen Bereich Asparaginsäure und Glutaminsäure negative Ladungen tragen und Lysin, Arginin und Histidin als Aminosäuren behandelt werden, die am Ladungszustand beteiligt sind.
| Ladung | Repräsentative Aminosäuren | Funktionelle Gruppen in der Seitenkette |
|---|---|---|
| Negativ (sauer) | Asparaginsäure, Glutaminsäure | Carboxylgruppe |
| Positiv (basisch) | Lysin, Arginin, Histidin | Aminogruppe, Guanidinogruppe, Imidazol |
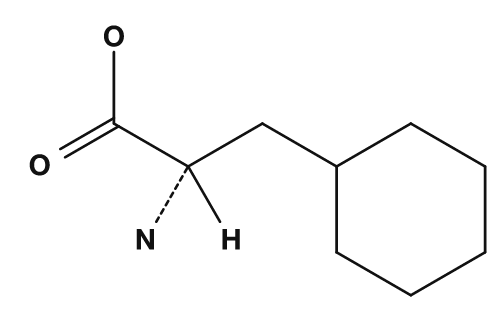
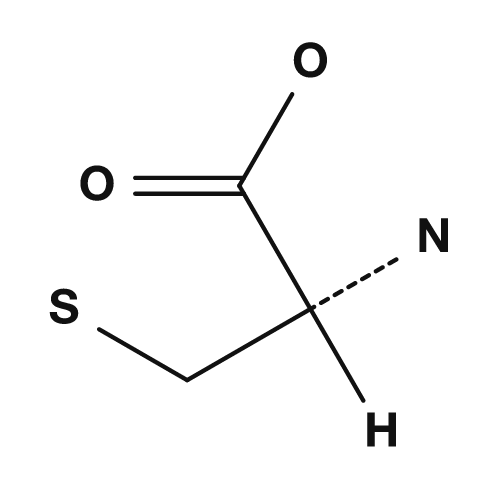
| Lysin | Phenylalanin | Cystein |
|---|---|---|
|
|
|
Aromatische Seitenketten
Zu den Aminosäuren mit aromatischen Seitenketten gehören Phenylalanin, Tyrosin und Tryptophan. Sie haben zyklische π-Elektronensysteme und sind in Strukturformeln relativ leicht zu erkennen. Tyrosin trägt eine phenolische Hydroxylgruppe und zeigt daher andere Eigenschaften als eine einfache hydrophobe aromatische Aminosäure. Tryptophan hat einen großen Indolring und ist auch im Hinblick auf die Proteinstruktur und Lichtabsorption wichtig.
Schwefelhaltige Seitenketten
Auch schwefelhaltige Seitenketten verdienen Aufmerksamkeit.
Cystein hat eine Thiolgruppe (-SH), und wenn zwei Cysteine oxidiert werden, können sie eine Disulfidbrücke bilden. Dies ist eine wichtige Bindung, die die dreidimensionale Struktur von Proteinen stabilisiert. Methionin hat eine Thioetherstruktur und ist auch als Aminosäure bekannt, die dem Startcodon AUG für die Translationsinitiation entspricht.
| Art der Seitenkette | Repräsentative Aminosäuren | Wichtige Punkte |
|---|---|---|
| Hydrophob | Valin, Leucin, Isoleucin | Sammeln sich im Inneren von Proteinen |
| Aromatisch | Phenylalanin, Tyrosin, Tryptophan | π-Elektronensystem, an UV-Absorption beteiligt |
| Schwefelhaltig | Cystein, Methionin | Disulfidbrücken, Bezug zum Startcodon AUG |
Wie man Strukturformeln liest
Beim Lernen von Seitenketten ist es einfacher zu verstehen, wenn man von der Strukturformel ausgeht, anstatt Aminosäurenamen und Eigenschaften getrennt auswendig zu lernen.
- Enthält Sauerstoff oder Stickstoff → tendiert zu polar
- Enthält eine Carboxylgruppe → tendiert zu sauer
- Enthält eine Amino- oder Guanidinogruppe → tendiert zu basisch
- Enthält viele Kohlenwasserstoffe → tendiert zu hydrophob
Zusammenfassung
Die Seitenkette einer Aminosäure ist der entscheidende Teil, der ihre Eigenschaften bestimmt. Unterschiede in der R-Gruppe erzeugen Merkmale wie Hydrophobie, Hydrophilie, Säurecharakter, Basencharakter, Aromatizität und Schwefelgehalt. Wenn man Strukturformeln betrachtet, hilft es, nicht nur auf das gemeinsame Grundgerüst, sondern auch darauf zu achten, welche Atome und funktionellen Gruppen in der Seitenkette enthalten sind, um die Eigenschaften von Aminosäuren leichter zu verstehen.