Es gibt 20 Standardaminosäuren, aus denen Proteine aufgebaut sind. Sie alle besitzen dasselbe Grundgerüst, unterscheiden sich aber in ihrer Seitenkette (R-Gruppe). NCBI Bookshelf nennt als die 20 proteinogenen Aminosäuren Alanin, Arginin, Asparagin, Asparaginsäure, Cystein, Glutaminsäure, Glutamin, Glycin, Histidin, Isoleucin, Leucin, Lysin, Methionin, Phenylalanin, Prolin, Serin, Threonin, Tryptophan, Tyrosin und Valin.
Beim Lernen der 20 Aminosäuren ist es einfacher, sie nach den Eigenschaften ihrer Seitenketten zu klassifizieren, anstatt nur die Namen auswendig zu lernen.
Zunächst eine Übersicht über alle 20.
| Kategorie | Wichtige Aminosäuren | Merkmale der Seitenkette |
|---|---|---|
| Unpolar | Glycin, Alanin, Valin, Leucin, Isoleucin, Prolin, Methionin | Mischen sich nur schlecht mit Wasser |
| Polar (ungeladen) | Serin, Threonin, Asparagin, Glutamin | Beteiligen sich häufig an Wasserstoffbrückenbindungen |
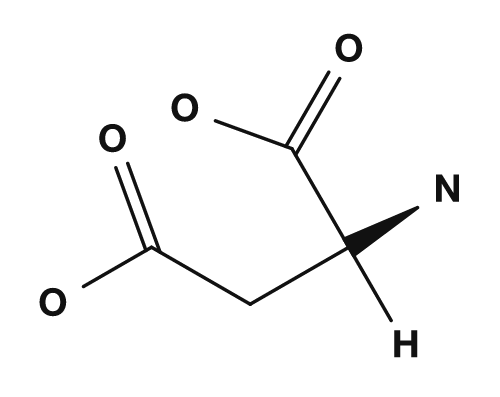
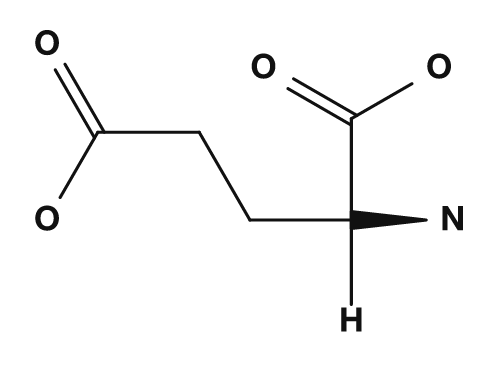
| Sauer | Asparaginsäure, Glutaminsäure | Bei physiologischem pH negativ geladen |
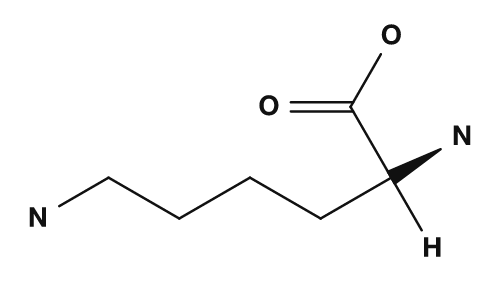
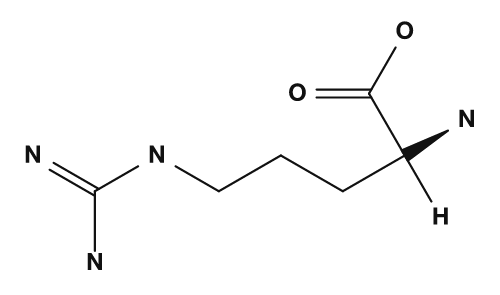
| Basisch | Lysin, Arginin, Histidin | Haben basische Seitenketten und neigen zu positiver Ladung |
| Aromatisch | Phenylalanin, Tyrosin, Tryptophan | Besitzen aromatische Ringe |
| Schwefelhaltig | Cystein, Methionin | Thiolgruppe bzw. Thioether |
| Sonderstruktur | Prolin | Sekundäres Amin, ringförmig |
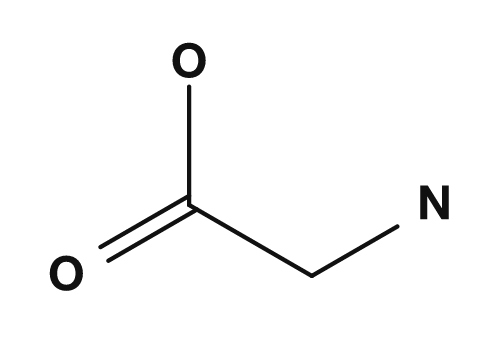
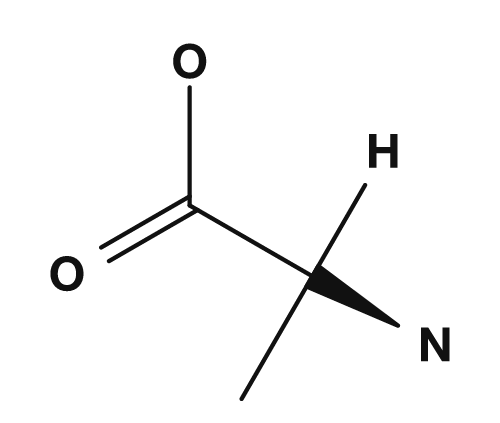
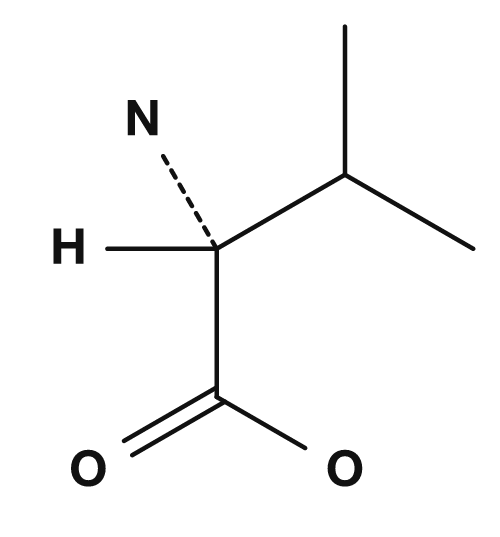
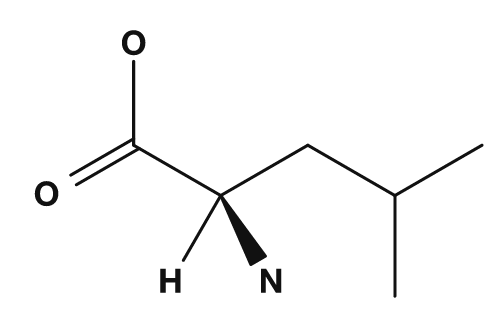
| Glycin | Alanin | Valin | Leucin | Isoleucin |
|---|---|---|---|---|
|
|
|
|
|
| Prolin | Methionin | Serin | Threonin | Cystein |
|---|---|---|---|---|
|
|
|
|
|
| Asparagin | Glutamin | Asparaginsäure | Glutaminsäure | Lysin |
|---|---|---|---|---|
|
|
|
|
|
| Arginin | Histidin | Phenylalanin | Tyrosin | Tryptophan |
|---|---|---|---|---|
|
|
|
|
|
Unpolare Aminosäuren
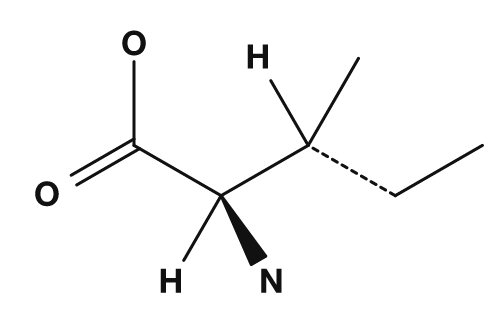
Zu den unpolaren Aminosäuren zählen Glycin, Alanin, Valin, Leucin, Isoleucin, Prolin und Methionin. Sie besitzen Seitenketten, die sich schlecht mit Wasser mischen, und neigen dazu, sich im Inneren von Proteinen zu sammeln. Insbesondere Valin, Leucin und Isoleucin werden auch als verzweigtkettige Aminosäuren bezeichnet.
Polare Aminosäuren (ungeladen)
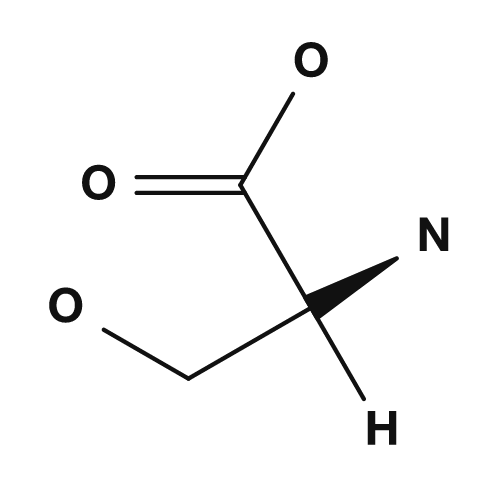
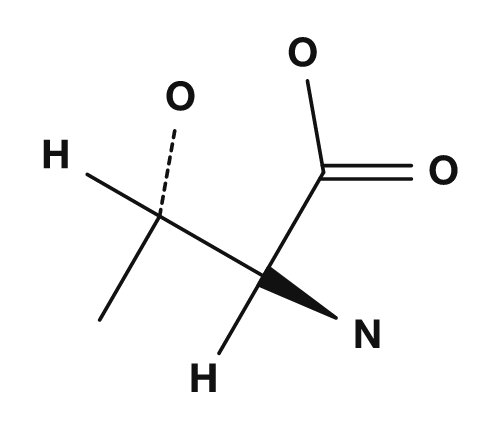
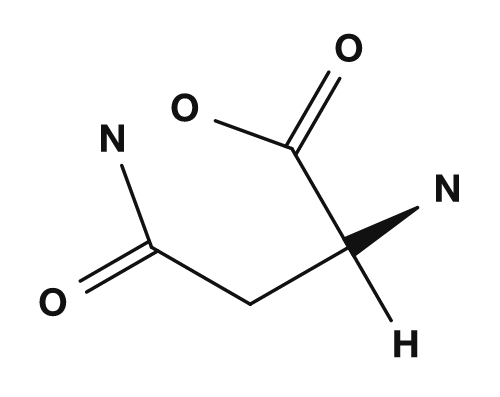
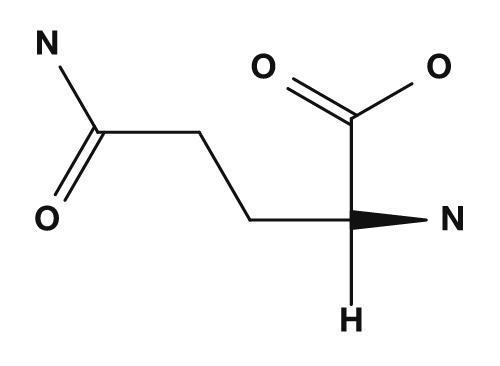
Zu den polaren, aber nicht leicht geladenen Aminosäuren gehören Serin, Threonin, Asparagin und Glutamin. Sie besitzen sauerstoff- oder stickstoffhaltige Seitenketten und können an Wasserstoffbrückenbindungen beteiligt sein. Sie wechselwirken an der Proteinoberfläche mit Wasser und spielen wichtige Rollen in den aktiven Zentren von Enzymen.
Saure und basische Aminosäuren
Saure Aminosäuren
Zu den sauren Aminosäuren zählen Asparaginsäure und Glutaminsäure. Sie besitzen in ihrer Seitenkette eine Carboxygruppe und tragen bei physiologischem pH häufig eine negative Ladung.
Basische Aminosäuren
Zu den basischen Aminosäuren gehören Lysin, Arginin und Histidin. Sie haben stickstoffhaltige Seitenketten und sind basisch. Insbesondere Lysin und Arginin tragen häufig eine positive Ladung, während Histidin als Seitenkette gilt, die je nach Bedingungen leicht protoniert werden kann. Sie sind auch wichtig, wenn man den isoelektrischen Punkt von Proteinen und die Wechselwirkungen mit DNA betrachtet.
Aromatische Aminosäuren
Zu den aromatischen Aminosäuren gehören Phenylalanin, Tyrosin und Tryptophan. Da sie aromatische Ringe besitzen, sind sie auch in der Strukturformel leicht zu erkennen. Tyrosin trägt ein phenolisches -OH, Tryptophan einen Indolring. Aromatische Aminosäuren sind auch für hydrophobe Wechselwirkungen in Proteinen und für die UV-Absorption von Bedeutung.
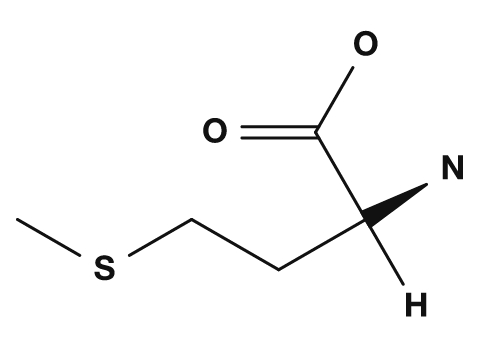
Schwefelhaltige Aminosäuren
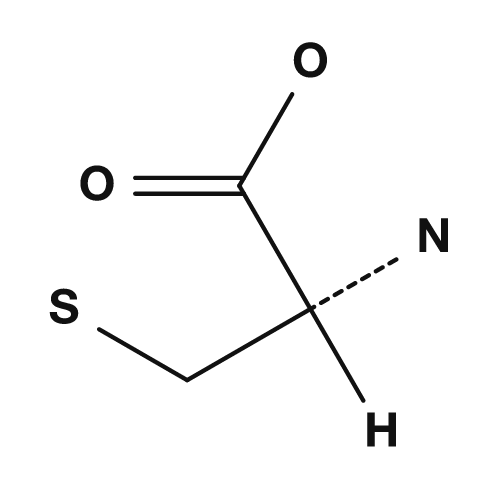
Zu den schwefelhaltigen Aminosäuren gehören Cystein und Methionin. Cystein trägt eine Thiolgruppe (-SH); wenn zwei Cysteine oxidiert werden, können sie eine Disulfidbrücke bilden. Diese Bindung ist wichtig, um die räumliche Struktur von Proteinen zu stabilisieren. Methionin ist eine Aminosäure mit Thioetherstruktur und ist als Aminosäure bekannt, die dem Startcodon AUG, also dem Beginn der Translation, entspricht.
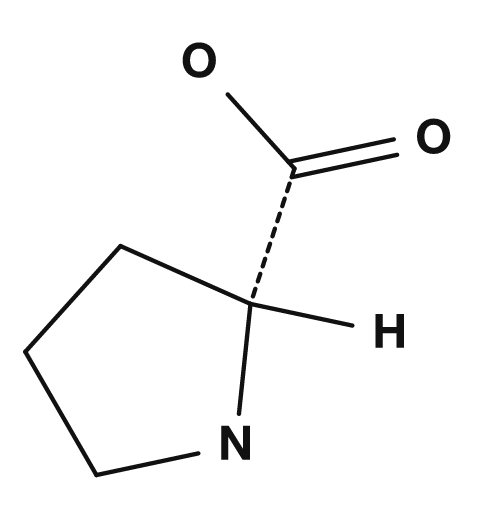
Prolin: eine besondere Struktur
Prolin ist etwas besonders. Bei den meisten Aminosäuren ist die Aminogruppe ein primäres Amin, bei Prolin aber bildet die Seitenkette mit der Aminogruppe einen Ring, sodass die Struktur eher einem sekundären Amin entspricht. Auch NCBI Bookshelf erklärt, dass Prolin im Unterschied zu anderen Aminosäuren eine sekundäre Aminogruppe besitzt. Aus diesem Grund ist Prolin an Krümmungen der Proteinhauptkette und an strukturellen Einschränkungen beteiligt.
Wie man Strukturformeln liest
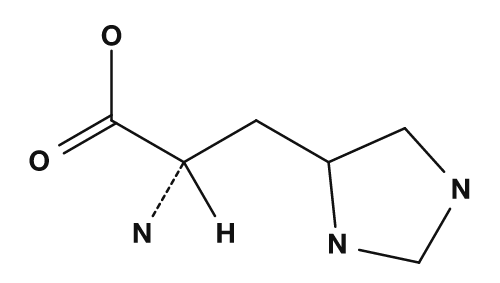
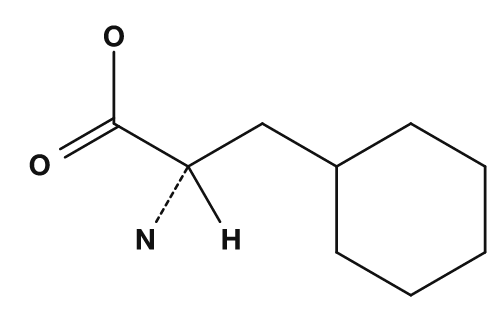
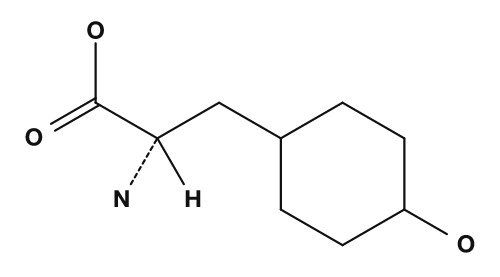
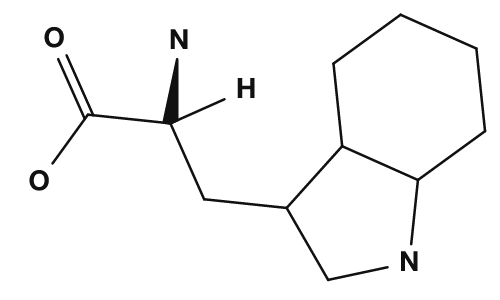
Beim Lernen der 20 Aminosäuren über Strukturformeln ist es hilfreich, zunächst das gemeinsame Grundgerüst zu finden und dann nur die R-Gruppen zu vergleichen. Anhand der folgenden Punkte zur R-Gruppe lassen sich die Eigenschaften einer Aminosäure abschätzen.
- Überwiegend Kohlenwasserstoffe → hydrophob
- Enthält Sauerstoff oder Stickstoff → polar
- Zusätzliche Carboxygruppe → sauer
- Zusätzliche Aminogruppe → basisch
- Aromatischer Ring vorhanden → aromatisch
Zusammenfassung
Die 20 Aminosäuren teilen sich dasselbe α-Aminosäure-Grundgerüst, ihre Eigenschaften ändern sich aber je nach Seitenkette. Anstatt nur die Namen auswendig zu lernen, lassen sich die Merkmale leichter aus den Strukturformeln ablesen, wenn man sie nach den Kategorien unpolar, polar, sauer, basisch, aromatisch, schwefelhaltig und Sonderstruktur ordnet.