Les acides aminés sont les unités de base qui constituent les protéines. Dans les organismes vivants, lorsque les protéines sont dégradées, elles deviennent des acides aminés, et ces acides aminés sont ensuite réutilisés pour synthétiser de nouvelles protéines, réparer les tissus et participer au métabolisme. MedlinePlus explique que les acides aminés et les protéines sont des éléments fondamentaux de la vie et que l'organisme utilise les acides aminés pour fabriquer des protéines.
Du point de vue de leur structure chimique, les acides aminés sont, comme leur nom l'indique, des composés possédant un groupe amine et un groupe carboxyle. Un acide aminé typique possède un atome de carbone central auquel sont liés un groupe amine, un groupe carboxyle, un atome d'hydrogène et une chaîne latérale. Cette chaîne latérale est également appelée groupe R et diffère selon l'acide aminé. NCBI Bookshelf explique que les acides aminés constituant les protéines possèdent un groupe α-carboxyle, un groupe α-amine et un groupe R, et que les différences au niveau du groupe R déterminent les propriétés de chaque acide aminé.
La structure chimique de base
La structure de base d'un acide aminé peut être représentée par la formule développée suivante.
H2N-CH(R)-COOH
Les différentes parties de cette formule correspondent à ce qui suit.
| Symbole | Nom |
|---|---|
CH |
carbone alpha |
NH2 |
groupe amine |
COOH |
groupe carboxyle |
R |
chaîne latérale (différente pour chaque acide aminé) |
Le type d'acide aminé est déterminé par le groupe R. Si R est un hydrogène, il s'agit de la glycine ; si c'est un groupe méthyle, de l'alanine ; si c'est un groupe benzyle, de la phénylalanine. Autrement dit, même si la partie commune reste identique, changer le groupe R donne un acide aminé différent.
| Acide aminé | Groupe R |
|---|---|
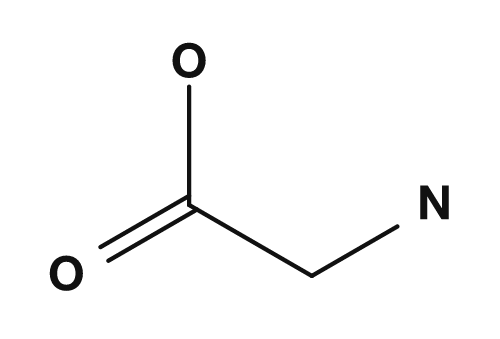
| Glycine | Hydrogène |
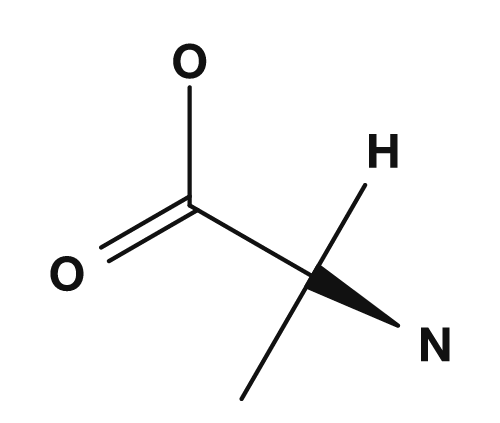
| Alanine | Groupe méthyle |
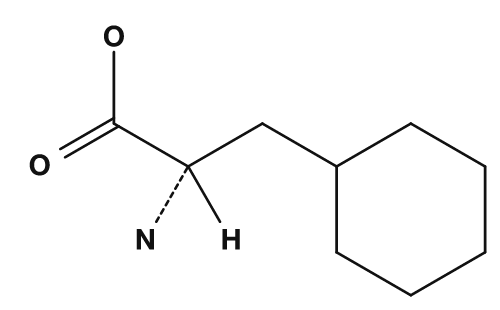
| Phénylalanine | Groupe benzyle |
| Glycine | Alanine | Phénylalanine |
|---|---|---|
|
|
|
La chaîne latérale (groupe R) détermine les propriétés
Pour comprendre les acides aminés à travers leur formule développée, il ne suffit pas de les retenir comme « les briques des protéines ». Le groupe amine est plutôt basique, le groupe carboxyle plutôt acide, et la chaîne latérale détermine des propriétés telles que l'hydrophobie, l'hydrophilie, l'acidité, la basicité et l'aromaticité. Ainsi, en observant la structure d'un acide aminé, on peut deviner s'il est plutôt soluble dans l'eau, s'il a tendance à se trouver à l'intérieur d'une protéine ou s'il porte facilement une charge.
Par exemple, la glycine n'a qu'un atome d'hydrogène comme chaîne latérale, ce qui en fait le plus petit acide aminé. PubChem décrit également la glycine comme l'acide aminé protéinogène le plus simple, avec un atome d'hydrogène comme chaîne latérale, et comme le seul acide aminé protéinogène achiral. À l'inverse, les acides aminés à chaîne latérale basique, comme la lysine et l'arginine, ont tendance à porter une charge positive dans les conditions physiologiques et participent aux interactions à la surface des protéines et avec d'autres molécules.
Quatre éléments pour comprendre la structure
Lors de l'apprentissage des acides aminés, il est plus important de comprendre d'abord le squelette commun que de mémoriser d'emblée les 20 noms. Une fois que vous savez identifier les quatre éléments suivants dans une formule développée, vous pouvez classer chaque acide aminé à partir de sa structure.
- Groupe amine (
-NH2) - Groupe carboxyle (
-COOH) - Carbone alpha (le carbone central)
- Groupe R (chaîne latérale)
Résumé
Les acides aminés sont des composés organiques qui possèdent un groupe amine et un groupe carboxyle. Dans les acides aminés qui constituent les protéines, le groupe amine, le groupe carboxyle, un hydrogène et un groupe R sont liés au carbone alpha. Les différences entre acides aminés sont principalement déterminées par le groupe R, et ces différences se traduisent aussi dans les propriétés et les fonctions des protéines.