Il existe de nombreux types d'acides aminés, mais la plupart des acides aminés majeurs qui composent les protéines sont des acides α-aminés. Un acide α-aminé est un acide aminé dans lequel le groupe amine et le groupe carboxyle sont liés au même carbone, à savoir le carbone α. NCBI Bookshelf explique que dans les acides α-aminés constituant les protéines, le groupe amine et le groupe fonctionnel acide carboxylique sont séparés par un seul atome de carbone, et qu'ils possèdent généralement un carbone chiral.
Structure d'un acide α-aminé
On commence par prendre comme référence le carbone de l'acide carboxylique. Le carbone voisin du groupe carboxyle -COOH est le carbone α. Un acide aminé dans lequel le groupe amine -NH2 est lié à ce carbone α est un acide α-aminé. La formule développée est la suivante.
H2N-CH(R)-COOH
Ici, le carbone de CH(R) est le carbone α. Quatre groupes sont liés à ce carbone : le groupe amine, le groupe carboxyle, un atome d'hydrogène et le groupe R. Les différences au niveau du groupe R donnent naissance à la glycine, à l'alanine, à la valine, à la phénylalanine, etc.
| Glycine | Alanine |
|---|---|
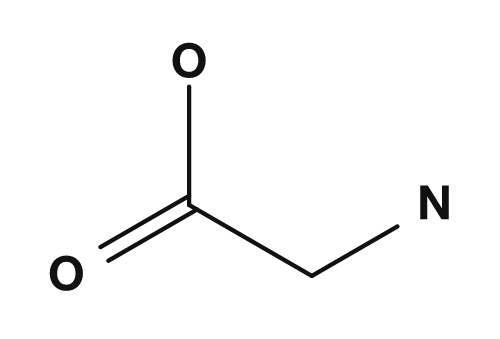
|
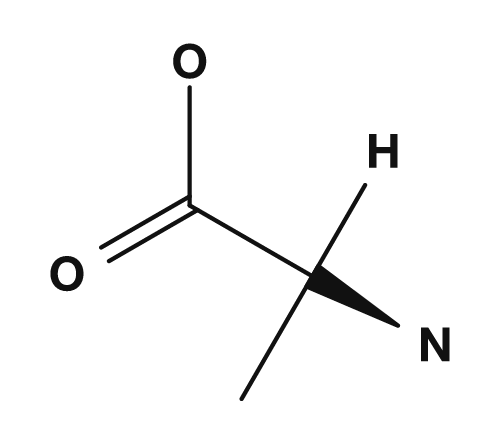
|
Pourquoi parle-t-on d'« α » ?
En chimie organique, on appelle parfois carbone α le carbone voisin d'un groupe fonctionnel donné, carbone β le suivant et carbone γ celui d'après. Dans le cas des acides aminés, le groupe amine est lié au carbone α, qui se trouve juste à côté du groupe carboxyle, d'où le nom d'acides α-aminés.
| Position du groupe amine | Nom |
|---|---|
| Carbone α (à côté du groupe carboxyle) | acide α-aminé |
| Carbone β (à deux carbones) | acide β-aminé |
| Carbone γ (à trois carbones) | acide γ-aminé |
Structure des protéines et acides α-aminés
Le fait que les acides aminés constituant les protéines soient des acides α-aminés est important pour comprendre la structure des protéines. Comme, autour du carbone α, le côté amine et le côté carboxyle sont reliés par des liaisons peptidiques, une structure répétitive régulière apparaît dans la chaîne principale de la protéine. NCBI Bookshelf explique que les protéines sont des polypeptides dans lesquels les acides aminés sont reliés par des liaisons peptidiques et que la séquence d'acides aminés détermine la structure primaire de la protéine.
Comment les reconnaître dans la formule développée
Lorsque l'on observe un acide α-aminé sur une formule développée, les trois points suivants facilitent l'identification.
- Repérer le groupe carboxyle
-COOH. - Identifier le carbone qui lui est voisin (le carbone α).
- Vérifier si le groupe amine est lié à ce carbone α.
Ces trois étapes permettent de déterminer si un composé est un acide α-aminé.
Relation avec la chiralité
Dans la plupart des acides α-aminés, le carbone α est un centre chiral. Comme quatre substituants différents sont liés au carbone α, il existe des stéréoisomères. Cependant, seule la glycine, dont le groupe R est un hydrogène, possède deux atomes d'hydrogène liés au carbone α et n'a donc pas de centre chiral. Ce point est très important lors de l'apprentissage de la stéréochimie des acides aminés. PubChem décrit également la glycine comme le seul acide aminé protéinogène achiral.
Résumé
Un acide α-aminé est un acide aminé dans lequel le groupe amine est lié au carbone α, situé à côté du groupe carboxyle. Les acides aminés standard qui composent les protéines sont principalement des acides α-aminés, et ce squelette commun est à l'origine des liaisons peptidiques et de la structure primaire des protéines. Lors de l'examen de la formule développée, il est important de vérifier la relation de position entre le groupe carboxyle, le carbone α et le groupe amine.