Es gibt viele Arten von Aminosäuren, aber die meisten der wichtigen Aminosäuren, aus denen Proteine aufgebaut sind, sind α-Aminosäuren. Eine α-Aminosäure ist eine Aminosäure, bei der die Aminogruppe und die Carboxygruppe an denselben Kohlenstoff gebunden sind, nämlich an den α-Kohlenstoff. NCBI Bookshelf erklärt, dass bei den α-Aminosäuren, aus denen Proteine bestehen, die Aminogruppe und die Carbonsäure-Funktionsgruppe durch ein einzelnes Kohlenstoffatom getrennt sind und dass sie in der Regel ein chirales Kohlenstoffatom besitzen.
Aufbau einer α-Aminosäure
Zunächst orientiert man sich am Kohlenstoff der Carbonsäure. Der Kohlenstoff neben der Carboxygruppe -COOH ist der α-Kohlenstoff. Eine Aminosäure, bei der die Aminogruppe -NH2 an diesen α-Kohlenstoff gebunden ist, ist eine α-Aminosäure. In der Strukturformel sieht das so aus.
H2N-CH(R)-COOH
Dabei ist der Kohlenstoff in CH(R) der α-Kohlenstoff. An diesem Kohlenstoff sind vier Gruppen gebunden: die Aminogruppe, die Carboxygruppe, ein Wasserstoffatom und die R-Gruppe. Durch Unterschiede in der R-Gruppe entstehen Glycin, Alanin, Valin, Phenylalanin und so weiter.
| Glycin | Alanin |
|---|---|
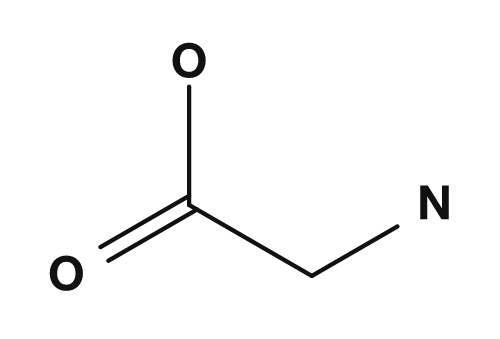
|
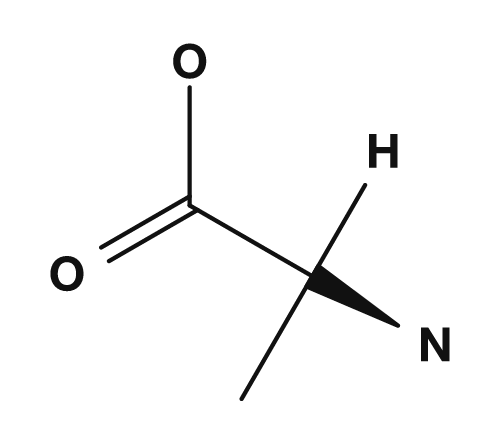
|
Warum heißt sie „α"?
In der organischen Chemie wird der Kohlenstoff neben einer bestimmten funktionellen Gruppe manchmal als α-Kohlenstoff bezeichnet, der nächste als β-Kohlenstoff und der übernächste als γ-Kohlenstoff. Bei Aminosäuren ist die Aminogruppe an den α-Kohlenstoff gebunden, der direkt neben der Carboxygruppe liegt, weshalb sie α-Aminosäuren genannt werden.
| Position der Aminogruppe | Bezeichnung |
|---|---|
| α-Kohlenstoff (neben der Carboxygruppe) | α-Aminosäure |
| β-Kohlenstoff (zwei Kohlenstoffe entfernt) | β-Aminosäure |
| γ-Kohlenstoff (drei Kohlenstoffe entfernt) | γ-Aminosäure |
Proteinstruktur und α-Aminosäuren
Dass die Aminosäuren, aus denen Proteine bestehen, α-Aminosäuren sind, ist für das Verständnis der Proteinstruktur wichtig. Da auf beiden Seiten des α-Kohlenstoffs die Amino- und die Carboxyseite über Peptidbindungen verknüpft werden, entsteht in der Hauptkette des Proteins eine regelmäßige, sich wiederholende Struktur. NCBI Bookshelf erklärt, dass Proteine Polypeptide sind, in denen Aminosäuren über Peptidbindungen verbunden sind, und dass die Aminosäuresequenz die Primärstruktur des Proteins bestimmt.
Erkennung in der Strukturformel
Wenn Sie eine α-Aminosäure in einer Strukturformel betrachten, helfen die folgenden drei Punkte beim Erkennen.
- Suchen Sie die Carboxygruppe
-COOH. - Identifizieren Sie den danebenstehenden Kohlenstoff (den α-Kohlenstoff).
- Prüfen Sie, ob die Aminogruppe an diesen α-Kohlenstoff gebunden ist.
Mit diesen drei Schritten lässt sich entscheiden, ob eine Verbindung eine α-Aminosäure ist.
Beziehung zur Chiralität
Bei den meisten α-Aminosäuren ist der α-Kohlenstoff ein Chiralitätszentrum. Da am α-Kohlenstoff vier verschiedene Substituenten gebunden sind, existieren Stereoisomere. Nur Glycin mit der R-Gruppe Wasserstoff besitzt zwei Wasserstoffatome am α-Kohlenstoff und hat daher kein Chiralitätszentrum. Dieser Punkt ist beim Erlernen der Stereochemie von Aminosäuren sehr wichtig. Auch PubChem beschreibt Glycin als die einzige achirale proteinogene Aminosäure.
Zusammenfassung
Eine α-Aminosäure ist eine Aminosäure, bei der die Aminogruppe an den α-Kohlenstoff, also den Kohlenstoff direkt neben der Carboxygruppe, gebunden ist. Die proteinogenen Standardaminosäuren sind hauptsächlich α-Aminosäuren, und dieses gemeinsame Grundgerüst ist die Grundlage für Peptidbindungen und die Primärstruktur von Proteinen. Beim Betrachten der Strukturformel ist es wichtig, die räumliche Beziehung zwischen Carboxygruppe, α-Kohlenstoff und Aminogruppe zu prüfen.