Aminosäuren existieren nicht nur einzeln, sondern verbinden sich miteinander zu Peptiden und Proteinen. Die Bindung, die in diesem Fall Aminosäuren miteinander verknüpft, ist die Peptidbindung. Laut NCBI Bookshelf sind Proteine Ketten von Aminosäuren, die durch Peptidbindungen verbunden sind, und die Aminosäuresequenz bestimmt die Primärstruktur.
| Glycin | Alanin |
|---|---|
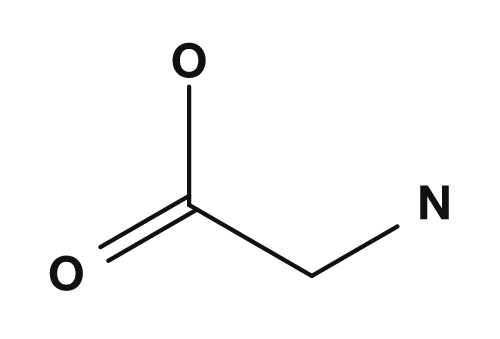
|
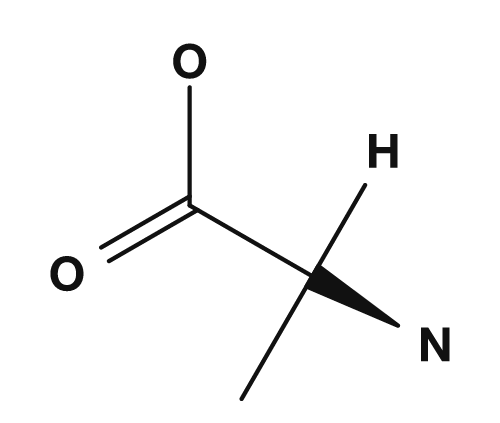
|
Bildung der Peptidbindung
Eine Peptidbindung ist eine Amidbindung, die entsteht, wenn die Carboxylgruppe einer Aminosäure mit der Aminogruppe einer anderen Aminosäure reagiert. Bei der Reaktion wird ein Wassermolekül abgespalten, weshalb sie als Kondensationsreaktion bezeichnet wird. Als Strukturformel ausgedrückt entsteht folgende Teilstruktur.
-CO-NH-
Dieses -CO-NH- ist die Peptidbindung. Da es sich um die Struktur handelt, die durch die Verbindung einer Carbonsäure mit einem Amin zu einem Amid entsteht, kann die Peptidbindung als eine Art Amidbindung betrachtet werden. Im Eintrag „Peptide" von NCBI Bookshelf werden Peptide als kurze Ketten von 2–50 Aminosäuren beschrieben, die durch Kondensationsreaktionen kovalent verbunden sind.
Arten von Peptidketten
Die Bezeichnung ändert sich je nach Anzahl der verknüpften Aminosäuren. In Molecular Biology of the Cell werden Proteine als lange Ketten aus 20 verschiedenen Aminosäuren beschrieben, die durch kovalente Peptidbindungen verbunden sind.
| Bezeichnung | Anzahl der Aminosäuren |
|---|---|
| Dipeptid | 2 |
| Tripeptid | 3 |
| Oligopeptid | Wenige bis etwa ein Dutzend |
| Polypeptid | Mehr als das |
| Protein | Gefaltete lange Polypeptidketten |
Ein wichtiges Merkmal der Peptidbindung: Partieller Doppelbindungscharakter
Ein wichtiges Merkmal der Peptidbindung ist, dass sie im Gegensatz zu einer gewöhnlichen Einfachbindung partiellen Doppelbindungscharakter besitzt. Dies liegt daran, dass das freie Elektronenpaar des Amidstickstoffs mit der Carbonylgruppe in Resonanz steht. Dadurch besitzt der Bereich um die Peptidbindung Planarität, und die Rotation ist eingeschränkt. Diese Eigenschaft ist sehr wichtig für das Verständnis der dreidimensionalen Struktur von Proteinen.
Hauptmerkmale der Peptidbindung:
- Eine Art Amidbindung (
-CO-NH-) - Wird durch eine Kondensationsreaktion (Abspaltung eines Wassermoleküls) gebildet
- Besitzt partiellen Doppelbindungscharakter
- Der Bereich um die Bindung weist Planarität auf, die Rotation ist eingeschränkt
N-Terminus und C-Terminus
Eine Peptidkette hat eine Direktionalität.
| Terminus | Verbleibende funktionelle Gruppe | Leserichtung |
|---|---|---|
| N-Terminus | Aminogruppe (-NH2) |
Beginn der Aminosäuresequenz |
| C-Terminus | Carboxylgruppe (-COOH) |
Ende der Aminosäuresequenz |
Die Aminosäuresequenz eines Proteins wird üblicherweise vom N-Terminus zum C-Terminus geschrieben. Wenn man diese Direktionalität versteht, lassen sich die Strukturformeln von Peptiden und Proteinen leichter lesen.
Identifizierung von Peptidbindungen in Strukturformeln
Um eine Peptidbindung in einer Strukturformel zu erkennen, sucht man nach dem -CO-NH--Teil. Da der Carbonylkohlenstoff an einen Stickstoff gebunden ist, hat er dieselbe Struktur wie ein Amid. Wenn jedoch auf beiden Seiten von Aminosäuren stammende α-Kohlenstoffe verbunden sind, wird sie als Peptidbindung behandelt.
Biologische Bedeutung
Die Peptidbindung ist für Lebewesen äußerst wichtig. Viele biologische Moleküle wie Enzyme, Antikörper, Hormone und Strukturproteine entstehen durch die Verknüpfung von Aminosäuren über Peptidbindungen. MedlinePlus erklärt ebenfalls, dass Aminosäuren Proteine bilden und für das Wachstum und die Reparatur von Körpergeweben verwendet werden.
Zusammenfassung
Eine Peptidbindung ist die -CO-NH--Bindung, die durch Kondensation zwischen der Carboxylgruppe einer Aminosäure und der Aminogruppe einer anderen entsteht. Die Peptidbindung ist eine Art Amidbindung und besitzt partiellen Doppelbindungscharakter, was auch die dreidimensionale Struktur von Proteinen beeinflusst. Durch die Verknüpfung von Aminosäuren über Peptidbindungen entstehen Peptide und Proteine.