단백질을 구성하는 20종류의 표준 아미노산 중에서 글리신은 특별한 존재입니다. 대부분의 아미노산은 키랄 중심을 가지고 D체와 L체 같은 입체이성질체를 고려해야 합니다. 그러나 글리신만은 광학 이성질체를 가지지 않습니다. 그 이유는 글리신의 곁사슬이 수소 원자이기 때문입니다.
α탄소의 치환기: 글리신과 다른 아미노산
일반적인 α-아미노산의 구조는 다음과 같이 나타낼 수 있습니다.
H2N-CH(R)-COOH
대부분의 아미노산에서는 α탄소에 아미노기, 카르복실기, 수소 원자, R기의 4종류의 서로 다른 치환기가 결합되어 있습니다. 이러한 탄소는 키랄 중심이 되어 거울상 이성질체를 가집니다.
그러나 글리신에서는 R기가 수소입니다. 따라서 α탄소에 결합된 치환기는 아미노기, 카르복실기, 수소, 수소가 됩니다. 수소가 2개 있기 때문에 4종류의 서로 다른 치환기가 되지 않습니다.
PubChem에서는 글리신을 곁사슬로 수소 원자를 가진 가장 단순한 단백질 구성 아미노산이며, 유일한 비키랄 단백질 구성 아미노산이라고 설명합니다. NCBI Bookshelf에서도 20종류의 단백질 구성 아미노산은 모두 L 이성질체이며, 글리신을 제외하고 α탄소에 키랄 중심을 가진다고 설명합니다.
글리신과 알라닌의 비교
| 아미노산 | α탄소의 치환기 | 키랄 중심 | 광학 이성질체 |
|---|---|---|---|
| 알라닌 (예) | NH2, COOH, H, CH3 |
있음 | D체·L체가 존재 |
| 글리신 | NH2, COOH, H, H |
없음 | 존재하지 않음 |
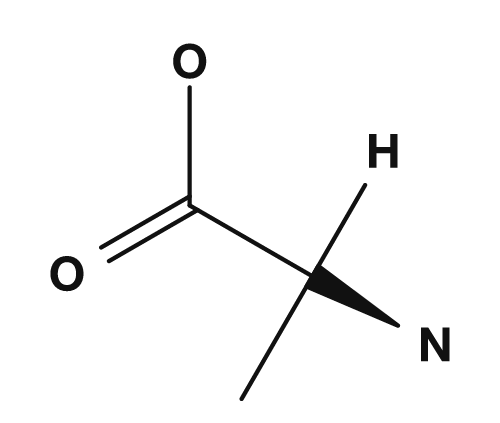
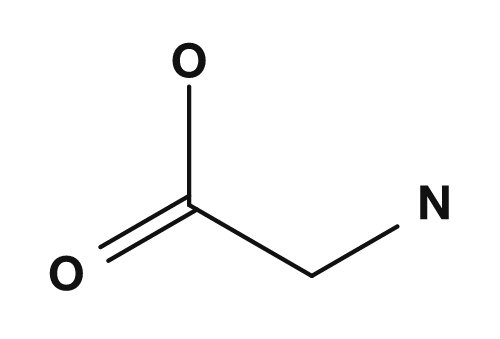
| 알라닌 | 글리신 |
|---|---|
|
|
키랄 중심과 광학 이성질체
키랄 중심을 가지지 않는다는 것은 글리신에는 D체와 L체의 구별이 없다는 것입니다. 알라닌이나 발린 등에서는 거울에 비친 것 같은 2가지 배치를 구별할 수 있지만, 글리신에서는 α탄소 주변에 같은 치환기가 2개 있기 때문에 거울상을 만들어도 원래 구조에 겹칠 수 있습니다. 이것이 글리신이 광학 이성질체를 가지지 않는 이유입니다.
구조식으로 확인
구조식으로 이 차이를 확인하면 이해하기 쉬워집니다.
- 알라닌: α탄소에
NH2,COOH,H,CH3가 결합 → 4개 모두 다름 → 키랄 - 글리신: α탄소에
NH2,COOH,H,H가 결합 → 수소가 2개 → 키랄 중심 없음
즉, 글리신의 특별함은 구조식을 보면 바로 이해할 수 있습니다.
단백질 구조에 대한 영향
글리신이 작다는 것은 단백질 구조에도 영향을 미칩니다. 곁사슬이 수소뿐이므로 다른 아미노산보다 입체적인 부피가 작아 단백질 주사슬이 비교적 자유롭게 움직일 수 있는 곳에 나타나기 쉽습니다. NCBI Bookshelf의 Molecular Biology of the Cell에서는 단백질의 3차원 구조는 아미노산 서열에 의해 결정되며, 곁사슬 사이의 상호작용이 접힘을 안정화한다고 설명합니다. 글리신의 작은 곁사슬은 이러한 입체 구조 속에서 독특한 역할을 합니다.
또한 글리신은 가장 단순한 아미노산이므로 아미노산의 기본 구조를 배우는 첫 번째 예로도 적합합니다. 단, 키랄성의 설명에서는 예외로 다루어야 합니다. 대부분의 아미노산은 키랄하지만 글리신만은 다르다는 점을 파악하는 것이 중요합니다.
키랄 중심의 성립 조건
글리신을 이해하면 키랄 중심의 조건도 자연스럽게 이해됩니다.
- 탄소가 4개의 결합을 가짐 (필요하지만 충분하지 않음)
- 4개의 치환기가 모두 다름 (이것이 필요조건)
글리신은 조건 2를 만족하지 않기 때문에 키랄 중심이 되지 않습니다. 단순히 탄소가 4개의 결합을 가지면 되는 것이 아닙니다. 결합된 치환기가 모두 달라야 합니다.
정리
글리신만이 광학 이성질체를 가지지 않는 이유는 곁사슬이 수소 원자이며, α탄소에 같은 수소가 2개 결합되어 있기 때문입니다. 따라서 α탄소는 4종류의 서로 다른 치환기를 가지지 못하며, 키랄 중심이 되지 않습니다. 글리신은 단백질 구성 아미노산 중 가장 단순하며, 유일한 비키랄 아미노산입니다.