아미노산을 이해하는 데 있어 가장 중요한 것은 곁사슬입니다. 곁사슬은 R기라고도 불리며, 아미노산마다 다른 부분입니다. 아미노산의 공통 골격은 거의 같지만, R기가 바뀌면 물에 잘 녹는지, 전하를 가지는지, 단백질 내부에 들어가기 쉬운지 등의 성질이 달라집니다. NCBI Bookshelf에서는 아미노산이 α-카르복시기, α-아미노기, R기를 가지며, R기의 차이가 각 아미노산의 고유한 성질을 결정한다고 설명하고 있습니다.
아미노산의 기본 구조는 다음과 같이 표현할 수 있습니다.
H2N-CH(R)-COOH
곁사슬의 기초: R기의 예
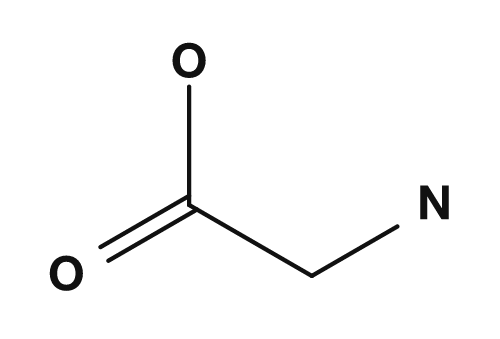
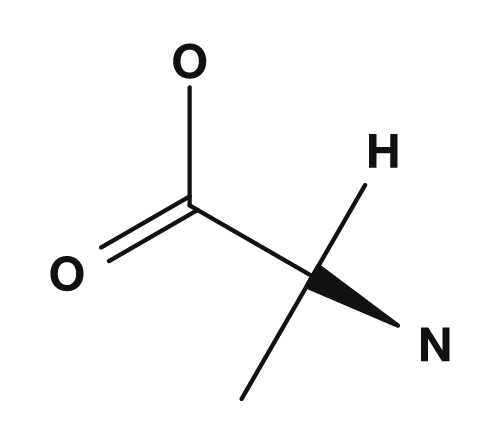
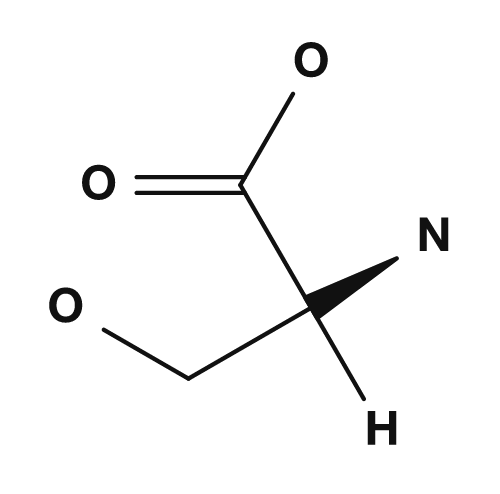
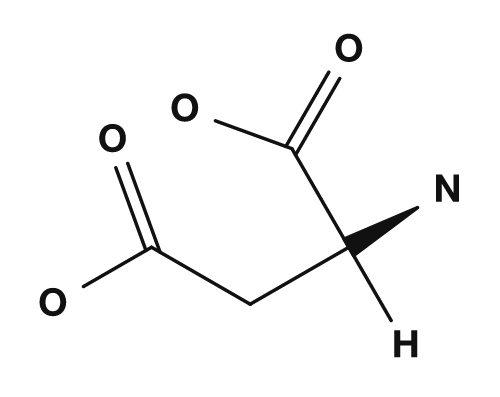
이 R 부분이 곁사슬입니다. 예를 들어 글리신에서 R기는 수소, 알라닌에서는 메틸기, 세린에서는 하이드록시메틸기, 아스파르트산에서는 카복시메틸기입니다. 이 작은 차이가 아미노산의 성질에 큰 영향을 미칩니다.
| 아미노산 | R기 | 특징 |
|---|---|---|
| 글리신 | 수소 | 가장 작은 아미노산, 비키랄성 |
| 알라닌 | 메틸기 | 단순한 비극성 |
| 세린 | 하이드록시메틸기 | 극성, 수소결합에 관여 |
| 아스파르트산 | 카복시메틸기 | 산성, 음전하를 띠기 쉬움 |
| 글리신 | 알라닌 | 세린 | 아스파르트산 |
|---|---|---|---|
|
|
|
|
물과의 친화성: 소수성과 친수성
곁사슬을 분류하는 가장 기본적인 관점은 물과의 친화성입니다.
- 탄화수소를 많이 포함하는 곁사슬은 소수성을 나타내기 쉽고, 단백질 내부에 모이기 쉬운 경향이 있습니다.
- 산소나 질소를 포함하는 곁사슬은 수소결합에 관여하기 쉽고 친수성을 가집니다.
단백질의 형태는 이러한 곁사슬 간의 상호작용에 의해 크게 좌우됩니다. NCBI Bookshelf의 Molecular Biology of the Cell에서는 소수성 곁사슬을 가진 아미노산이 단백질 내부에 모이기 쉽고, 비공유 결합성 상호작용이 접힘 구조를 안정화한다고 설명하고 있습니다.
산성, 염기성 곁사슬
다음으로 중요한 것은 산성, 염기성 곁사슬입니다.
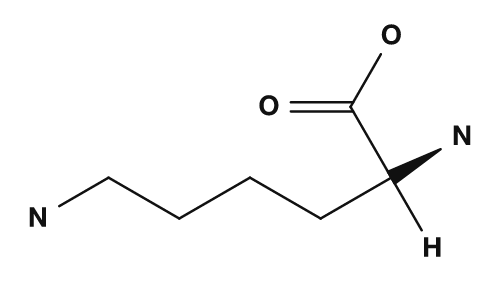
아스파르트산과 글루탐산은 곁사슬에 카복시기를 가지며, 생리학적 pH에서는 음전하를 띠기 쉬운 아미노산입니다. 라이신, 아르기닌, 히스티딘은 곁사슬에 염기성 질소를 포함합니다. 특히 라이신과 아르기닌은 양전하를 띠기 쉽고, 히스티딘은 조건에 따라 양성자화되기 쉬운 곁사슬로 중요합니다. PMC 게재 논문에서도 중성 부근에서는 아스파르트산과 글루탐산이 음전하, 라이신, 아르기닌, 히스티딘이 전하 상태에 관여하는 아미노산으로 다뤄진다고 설명하고 있습니다.
| 전하 | 대표 아미노산 | 곁사슬의 작용기 |
|---|---|---|
| 음전하 (산성) | 아스파르트산, 글루탐산 | 카복시기 |
| 양전하 (염기성) | 라이신, 아르기닌, 히스티딘 | 아미노기, 구아니디노기, 이미다졸 |
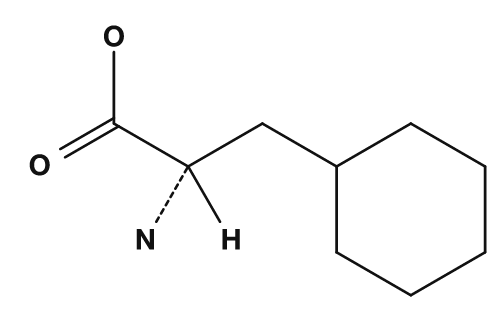
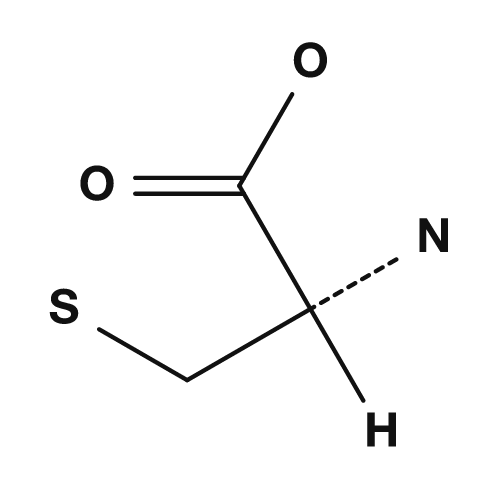
| 라이신 | 페닐알라닌 | 시스테인 |
|---|---|---|
|
|
|
방향족 곁사슬
방향족 곁사슬을 가진 아미노산으로는 페닐알라닌, 티로신, 트립토판이 있습니다. 이들은 고리형의 π 전자계를 가지며, 구조식에서도 비교적 눈에 띕니다. 티로신은 페놀성 하이드록시기를 가지므로 단순한 소수성 방향족과는 다른 성질을 나타냅니다. 트립토판은 큰 인돌 고리를 가지며, 단백질 구조나 빛 흡수의 관점에서도 중요합니다.
황을 포함하는 곁사슬
황을 포함하는 곁사슬에도 주목할 필요가 있습니다.
시스테인은 싸이올기 (-SH)를 가지며, 두 개의 시스테인이 산화되면 이황화 결합을 만들 수 있습니다. 이는 단백질의 입체 구조를 안정화하는 중요한 결합입니다. 메티오닌은 싸이오에테르 구조를 가지며, 번역 개시에 해당하는 개시 코돈 AUG와 관련된 아미노산으로도 잘 알려져 있습니다.
| 곁사슬의 종류 | 대표 아미노산 | 핵심 |
|---|---|---|
| 소수성 | 발린, 류신, 이소류신 | 단백질 내부에 모이기 쉬움 |
| 방향족 | 페닐알라닌, 티로신, 트립토판 | π 전자계, 자외선 흡수에 관여 |
| 황 함유 | 시스테인, 메티오닌 | 이황화 결합, 개시 코돈 AUG와의 관계 |
구조식에서 읽어내는 방법
곁사슬을 학습할 때는 아미노산 이름과 성질을 따로 외우는 것보다 구조식에서 생각하는 것이 이해하기 쉽습니다.
- 산소나 질소가 있다 → 극성을 가지기 쉬움
- 카복시기가 있다 → 산성이 되기 쉬움
- 아미노기나 구아니디노기가 있다 → 염기성이 되기 쉬움
- 탄화수소가 많다 → 소수성이 되기 쉬움
정리
아미노산의 곁사슬은 그 아미노산의 성질을 결정하는 중요한 부분입니다. R기의 차이에 의해 소수성, 친수성, 산성, 염기성, 방향족성, 황 함유 등의 특징이 생깁니다. 구조식을 볼 때는 공통 골격뿐만 아니라 곁사슬에 어떤 원자나 작용기가 포함되어 있는지에 주목하면 아미노산의 성질을 이해하기 쉬워집니다.