아미노산에는 다양한 종류가 있지만, 단백질을 구성하는 주요 아미노산은 대부분 α-아미노산입니다. α-아미노산이란 아미노기와 카르복실기가 같은 탄소, 즉 α 탄소에 결합되어 있는 아미노산을 말합니다. NCBI Bookshelf는 단백질을 구성하는 α-아미노산은 아미노기와 카르복실산 작용기가 하나의 탄소 원자를 사이에 두고 배치되며, 일반적으로 키랄 탄소를 가진다고 설명합니다.
α-아미노산의 구조
먼저 카르복실산의 탄소를 기준으로 생각합니다. 카르복실기 -COOH의 옆에 있는 탄소가 α 탄소입니다. 그 α 탄소에 아미노기 -NH2가 결합되어 있는 것이 α-아미노산입니다. 구조식으로는 다음과 같이 나타낼 수 있습니다.
H2N-CH(R)-COOH
여기서 CH(R)의 탄소가 α 탄소입니다. 이 탄소에는 아미노기, 카르복실기, 수소 원자, R기 네 가지가 결합되어 있습니다. R기가 달라지면서 글리신, 알라닌, 발린, 페닐알라닌 등의 차이가 생깁니다.
| 글리신 | 알라닌 |
|---|---|
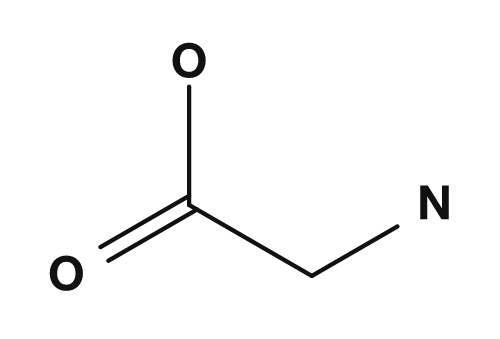
|
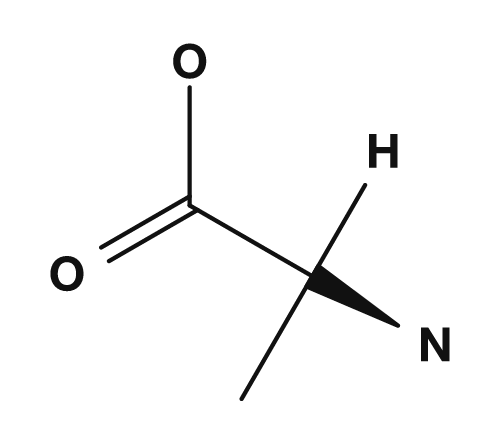
|
왜 "α"라고 부르는가
유기화학에서는 어떤 작용기 옆의 탄소를 α 탄소, 그다음 탄소를 β 탄소, 그 다음을 γ 탄소라고 부르기도 합니다. 아미노산의 경우 카르복실기를 기준으로 바로 옆의 α 탄소에 아미노기가 결합되어 있기 때문에 α-아미노산이라고 부릅니다.
| 아미노기의 위치 | 명칭 |
|---|---|
| α 탄소 (카르복실기 옆) | α-아미노산 |
| β 탄소 (두 칸 옆) | β-아미노산 |
| γ 탄소 (세 칸 옆) | γ-아미노산 |
단백질의 구조와 α-아미노산
단백질을 구성하는 아미노산이 α-아미노산이라는 사실은 단백질의 구조를 이해하는 데 매우 중요합니다. α 탄소를 중심으로 아미노기 쪽과 카르복실기 쪽이 펩타이드 결합으로 이어지기 때문에, 단백질의 주쇄에는 일정한 반복 구조가 생깁니다. NCBI Bookshelf는 단백질이 아미노산이 펩타이드 결합으로 연결된 폴리펩타이드이며, 아미노산 서열이 단백질의 1차 구조를 결정한다고 설명합니다.
구조식에서 구분하는 방법
α-아미노산을 구조식에서 살펴볼 때는 다음 세 가지를 확인하면 알기 쉽습니다.
- 카르복실기
-COOH를 찾는다. - 그 옆의 탄소(α 탄소)를 확인한다.
- 그 α 탄소에 아미노기가 결합되어 있는지 본다.
이 세 단계로 어떤 화합물이 α-아미노산인지 판단할 수 있습니다.
키랄 중심과의 관계
대부분의 α-아미노산에서는 α 탄소가 키랄 중심이 됩니다. α 탄소에는 네 가지 서로 다른 치환기가 결합되어 있기 때문에 입체이성질체가 존재합니다. 다만 글리신만은 R기가 수소이고, α 탄소에 수소가 두 개 결합되어 있는 형태이기 때문에 키랄 중심을 가지지 않습니다. 이 점은 아미노산의 입체화학을 학습할 때 매우 중요합니다. PubChem에서도 글리신은 유일한 비키랄성 단백질 구성 아미노산으로 설명됩니다.
정리
α-아미노산이란 카르복실기 옆에 있는 α 탄소에 아미노기가 결합된 아미노산을 말합니다. 단백질을 구성하는 표준 아미노산은 주로 α-아미노산이며, 이 공통 골격이 펩타이드 결합과 단백질의 1차 구조로 이어집니다. 구조식을 볼 때는 카르복실기, α 탄소, 아미노기의 위치 관계를 확인하는 것이 중요합니다.