在构成蛋白质的20种标准氨基酸中,甘氨酸是特殊的存在。大多数氨基酸具有手性中心,需要考虑D型和L型等立体异构体。然而,只有甘氨酸没有光学异构体。原因在于甘氨酸的侧链是氢原子。
α碳的取代基:甘氨酸与其他氨基酸
一般α-氨基酸的结构可以表示为:
H2N-CH(R)-COOH
大多数氨基酸的α碳与氨基、羧基、氢原子、R基这4种不同取代基结合。这样的碳成为手性中心,具有对映异构体。
然而,甘氨酸的R基是氢。因此,与α碳结合的取代基为氨基、羧基、氢、氢。由于有两个氢,4种取代基并不全部不同。
PubChem 描述甘氨酸为侧链是氢原子的最简单蛋白质构成氨基酸,是唯一的非手性蛋白质构成氨基酸。NCBI Bookshelf 也解释说,20种蛋白质构成氨基酸都是L异构体,除甘氨酸外α碳都有手性中心。
甘氨酸与丙氨酸的比较
| 氨基酸 | α碳的取代基 | 手性中心 | 光学异构体 |
|---|---|---|---|
| 丙氨酸(例) | NH2、COOH、H、CH3 |
有 | 存在D型·L型 |
| 甘氨酸 | NH2、COOH、H、H |
无 | 不存在 |
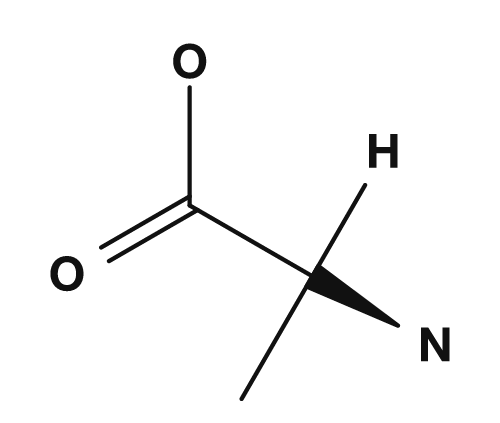
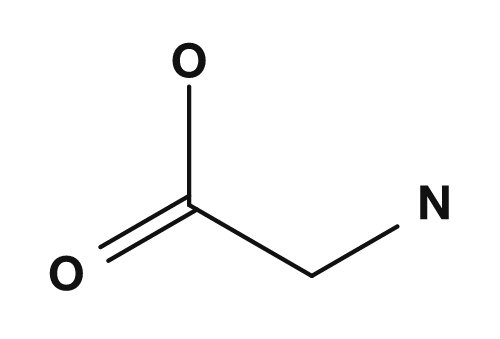
| 丙氨酸 | 甘氨酸 |
|---|---|
|
|
手性中心与光学异构体
没有手性中心意味着甘氨酸没有D型和L型的区别。对于丙氨酸和缬氨酸等氨基酸,可以区分互为镜像的两种构型,但甘氨酸的α碳周围有两个相同的取代基,因此镜像可以与原来的结构重叠。这就是甘氨酸没有光学异构体的原因。
从结构式确认
通过结构式确认这一区别会更容易理解。
- 丙氨酸:α碳与
NH2、COOH、H、CH3结合 → 4个全部不同 → 手性 - 甘氨酸:α碳与
NH2、COOH、H、H结合 → 有两个氢 → 没有手性中心
也就是说,甘氨酸的特殊性从结构式就能立刻理解。
对蛋白质结构的影响
甘氨酸的小体积也影响蛋白质结构。由于侧链只有氢,甘氨酸比其他氨基酸空间位阻更小,容易出现在蛋白质主链可以相对自由运动的位置。NCBI Bookshelf 的 Molecular Biology of the Cell 解释说,蛋白质的三维结构由氨基酸序列决定,侧链间的相互作用稳定了折叠结构。甘氨酸的小侧链在这样的立体结构中具有独特的作用。
此外,甘氨酸是最简单的氨基酸,因此也适合作为学习氨基酸基本结构的第一个例子。但在解释手性时,必须作为例外来处理。重要的是理解大多数氨基酸是手性的,而甘氨酸是特殊的。
手性中心的成立条件
理解甘氨酸也能自然地理解手性中心的条件。
- 碳有4个键(必要但不充分)
- 4个取代基全部不同(这是必要条件)
甘氨酸不满足条件2,因此不能成为手性中心。单纯地拥有4个键的碳并不足够。结合的取代基必须全部不同。
总结
甘氨酸没有光学异构体的原因是侧链是氢原子,α碳上结合了两个相同的氢。因此,α碳没有4种不同的取代基,不能成为手性中心。甘氨酸是蛋白质构成氨基酸中最简单的,是唯一的非手性氨基酸。