大多数氨基酸都有立体异构体。原因在于α碳成为手性中心。手性中心是指与四种不同取代基结合的碳原子。在大多数构成蛋白质的α-氨基酸中,α碳与氨基、羧基、氢原子和侧链R基结合,因此成为手性中心。NCBI Bookshelf 解释说,构成蛋白质的氨基酸是α-氨基酸,除甘氨酸外,α碳都有手性中心。
D型和L型的表示法
氨基酸立体化学中常见的表示法是D型和L型。D/L表示法是以甘油醛为基准表示相对构型的方法。构成蛋白质的标准氨基酸基本上都是L-氨基酸。NCBI Bookshelf 也说明,构成蛋白质的20种氨基酸都是L异构体。
D/L表示法与R/S表示法的区别
D/L表示法与R/S表示法并不相同。
| 表示体系 | 基准 | 蛋白质构成氨基酸 | 例外 |
|---|---|---|---|
| D/L表示法 | 以甘油醛为基准的相对构型 | L型 | 甘氨酸(无手性中心) |
| R/S表示法 | 基于CIP优先顺序规则的绝对构型 | 多为S构型 | 半胱氨酸(R构型) |
D/L是基于历史相对构型的表示法,R/S是基于CIP优先顺序规则的绝对构型。大多数L-氨基酸具有S构型,但半胱氨酸是例外——其侧链含有硫,导致优先顺序改变,例外地具有R构型。NCBI Bookshelf 也说明,除甘氨酸和半胱氨酸外的标准氨基酸在R/S表示法中为S构型,而半胱氨酸因其含硫的R基而具有R构型。
从结构式确认手性中心
在结构式中寻找手性中心时,要关注α碳。如果与该碳结合的4个取代基全部不同,则为手性中心。
| 氨基酸 | α碳的取代基 | 手性中心 |
|---|---|---|
| 丙氨酸 | NH2、COOH、H、CH3 |
有(4种全部不同) |
| 甘氨酸 | NH2、COOH、H、H |
无(有两个氢) |
| 丙氨酸 | 甘氨酸 | 半胱氨酸 |
|---|---|---|
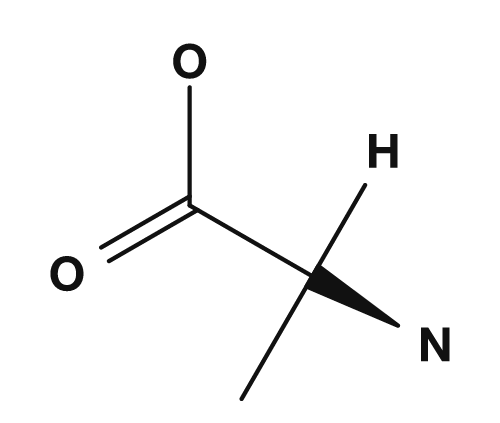
|
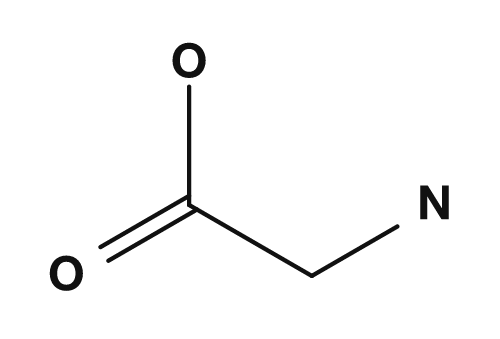
|
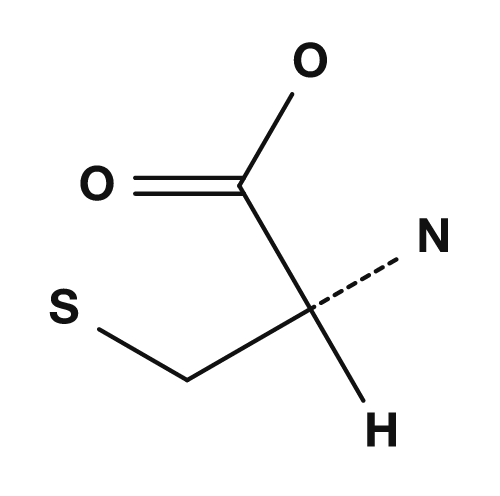
|
丙氨酸中,α碳与 NH2、COOH、H、CH3 结合。4种全部不同,因此丙氨酸是手性的。而甘氨酸的R基是氢,α碳与 NH2、COOH、H、H 结合,不构成4种,因此没有手性中心。PubChem 也说明,甘氨酸的侧链为氢原子,是唯一的非手性蛋白质构成氨基酸。
D型·L型与旋光方向
D型和L型是对映异构体(镜像异构体)的关系。具有相同分子式、相同结合关系,但空间排列互为镜像且不能重叠的一对分子称为对映异构体。在氨基酸中,这种立体配置的差异对与生物分子的相互作用有很大影响。生体内的酶和受体具有三维结构,因此能够区分L型和D型。
学习氨基酸的D/L表示法时,重要的是不要简单地认为"L就是左旋性"或"D就是右旋性"。D/L表示法并不直接表示旋光方向。旋光方向是实验测量的性质,用 + 或 - 表示。D/L是表示结构上相对构型的符号。
结构式学习要点
在结构式学习中,首先确认α碳是否有4种不同的取代基是第一步。
- 确认α碳是否有4种不同的取代基
- 甘氨酸例外地没有手性中心
- 构成蛋白质的氨基酸基本上是L型
- D/L表示法与R/S表示法是不同的表示体系
- 半胱氨酸是L型却具有R构型的例外
总结
大多数氨基酸因α碳具有4种不同的取代基而具有手性。构成蛋白质的标准氨基酸基本上是L型,只有甘氨酸因α碳上有两个相同的氢而没有手性中心。D/L表示法与R/S表示法是不同的体系,特别是半胱氨酸需要作为例外来理解。