タンパク質を構成する20種類の標準アミノ酸の中で,グリシンは特別な存在です.多くのアミノ酸はキラル中心を持ち,D体とL体のような立体異性体を考える必要があります.しかし,グリシンだけは光学異性体を持ちません.その理由は,グリシンの側鎖が水素原子だからです.
α炭素の置換基:グリシンと他のアミノ酸
一般的なα-アミノ酸の構造は,次のように表せます.
H2N-CH(R)-COOH
多くのアミノ酸では,α炭素にアミノ基,カルボキシ基,水素原子,R基の4種類の異なる置換基が結合しています.このような炭素はキラル中心になり,鏡像異性体を持ちます.
ところが,グリシンではR基が水素です.そのため,α炭素に結合している置換基は,アミノ基,カルボキシ基,水素,水素になります.水素が2つあるため,4種類の異なる置換基にはなりません.
PubChemでは,グリシンは側鎖として水素原子を持つ最も単純なタンパク質構成アミノ酸であり,唯一のアキラルなタンパク質構成アミノ酸と説明されています. NCBI Bookshelfでも,20種類のタンパク質構成アミノ酸はすべてL異性体であり,グリシンを除いてα炭素にキラル中心を持つと説明されています.
グリシンとアラニンの比較
| アミノ酸 | α炭素の置換基 | キラル中心 | 光学異性体 |
|---|---|---|---|
| アラニン(例) | NH2,COOH,H,CH3 |
あり | D体・L体が存在 |
| グリシン | NH2,COOH,H,H |
なし | 存在しない |
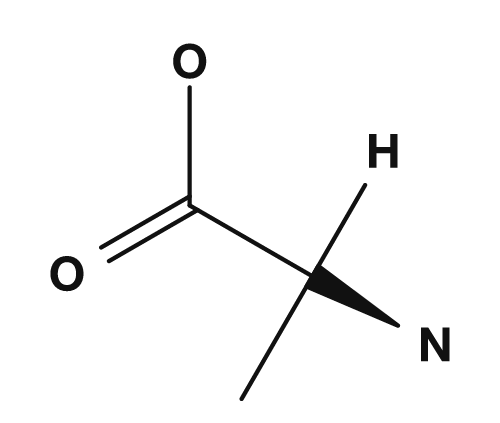
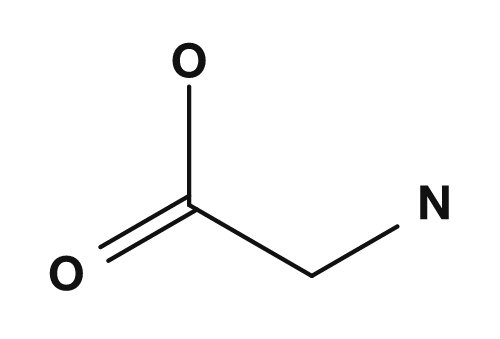
| アラニン | グリシン |
|---|---|
|
|
キラル中心と光学異性体
キラル中心を持たないということは,グリシンにはD体やL体の区別がないということです.アラニンやバリンなどでは,鏡に映したような2つの配置を区別できますが,グリシンではα炭素の周囲に同じ置換基が2つあるため,鏡像を作っても元の構造と重ね合わせることができます.これが,グリシンが光学異性体を持たない理由です.
構造式での確認
構造式でこの違いを確認すると分かりやすくなります.
- アラニン:α炭素に
NH2,COOH,H,CH3が結合 → 4つすべてが異なる → キラル - グリシン:α炭素に
NH2,COOH,H,Hが結合 → 水素が2つ → キラル中心を持たない
つまり,グリシンの特別さは,構造式を見ればすぐに理解できます.
タンパク質の構造への影響
グリシンが小さいことは,タンパク質の構造にも影響します.側鎖が水素だけなので,他のアミノ酸よりも立体的なかさばりが少なく,タンパク質の主鎖が比較的自由に動ける場所に現れやすいです.NCBI BookshelfのMolecular Biology of the Cellでは,タンパク質の三次元構造はアミノ酸配列によって決まり,側鎖どうしの相互作用が折りたたみを安定化すると説明されています. グリシンの小さな側鎖は,こうした立体構造の中で独特の役割を持ちます.
また,グリシンは最も単純なアミノ酸であるため,アミノ酸の基本構造を学ぶ最初の例としても適しています.ただし,キラリティの説明では例外として扱う必要があります.ほとんどのアミノ酸はキラルだが,グリシンだけは違う,という点を押さえることが大切です.
キラル中心の成立条件
グリシンを理解すると,キラル中心の条件も自然に理解できます.
- 炭素が4つの結合を持つ(必要だが十分ではない)
- 4つの置換基がすべて異なる(これが必要条件)
グリシンは条件2を満たさないため,キラル中心にならない.単に炭素が4本の結合を持っていればよいわけではありません.結合している置換基がすべて異なることが必要です.
まとめ
グリシンだけが光学異性体を持たない理由は,側鎖が水素原子であり,α炭素に同じ水素が2つ結合しているからです.そのため,α炭素は4種類の異なる置換基を持たず,キラル中心になりません.グリシンは,タンパク質構成アミノ酸の中で最も単純で,唯一のアキラルなアミノ酸です.