アミノ酸は,pHによって電荷の状態が変わります.酸性条件では正に帯電しやすく,塩基性条件では負に帯電しやすくなります.この電荷の変化を理解するうえで重要なのが,等電点です.等電点は,分子全体の正電荷と負電荷がつり合い,正味の電荷が0になるpHとして理解できます.IUPAC Gold Bookでは,等電状態は多価両性イオン,特にタンパク質が電気泳動を示さない状態として説明されています.
pHと電荷の変化
アミノ酸の基本構造には,アミノ基とカルボキシ基があります.
- 酸性条件では,アミノ基はプロトンを受け取って
-NH3+になりやすく,カルボキシ基は-COOHの形をとりやすくなります. - 塩基性条件では,カルボキシ基はプロトンを失って
-COO-になり,アミノ基も-NH2に近い状態になります. - 中間のpHでは,
-NH3+と-COO-を同時に持つ形(双性イオン)が多くなります.
| pH条件 | アミノ基の状態 | カルボキシ基の状態 | 正味の電荷 |
|---|---|---|---|
| 酸性(低pH) | -NH3+(正電荷) |
-COOH(中性) |
正 |
| 等電点付近 | -NH3+(正電荷) |
-COO-(負電荷) |
0(双性イオン) |
| 塩基性(高pH) | -NH2(中性) |
-COO-(負電荷) |
負 |
等電点とはどんな状態か
最も単純なアミノ酸であるグリシンを例に考えると,酸性側では全体として正電荷を持ちやすく,塩基性側では負電荷を持ちやすくなります.その途中に,正味の電荷が0になるpHがあります.これがグリシンの等電点です.
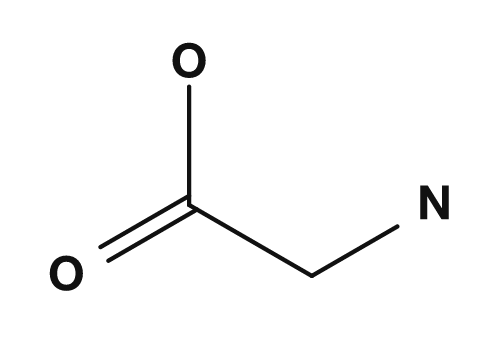
等電点を理解するときには,「電荷がまったくない」というよりも,正電荷と負電荷がつり合っている状態と考える方が正確です.アミノ酸は中性付近で双性イオンとして存在しやすく,分子内に正電荷と負電荷を同時に持ちます.PubChemでは,L-システイニルグリシンの双性イオンについて,あるヒドロキシ基からアミノ基へプロトンが移動した結果として生じ,pH 7.3で主要な微小化学種であると説明されています.
側鎖が等電点に影響する
等電点は,側鎖の種類によって変わります.
- 側鎖にカルボキシ基を持つアスパラギン酸やグルタミン酸は,負電荷を帯びやすいため等電点が低くなります.
- リシンやアルギニンのように塩基性側鎖を持つアミノ酸は,正電荷を帯びやすく,等電点が高くなります.
PMC掲載論文では,タンパク質のpIは正味電荷が0になるpHとして定義され,アミノ酸組成と各側鎖のpKa値に大きく依存すると説明されています.
| 側鎖の性質 | 代表アミノ酸 | 等電点への影響 |
|---|---|---|
| 側鎖にカルボキシ基(酸性) | アスパラギン酸,グルタミン酸 | 等電点が低くなる |
| 側鎖に塩基性窒素(塩基性) | リシン,アルギニン,ヒスチジン | 等電点が高くなる |
| アスパラギン酸 | グルタミン酸 | リシン |
|---|---|---|
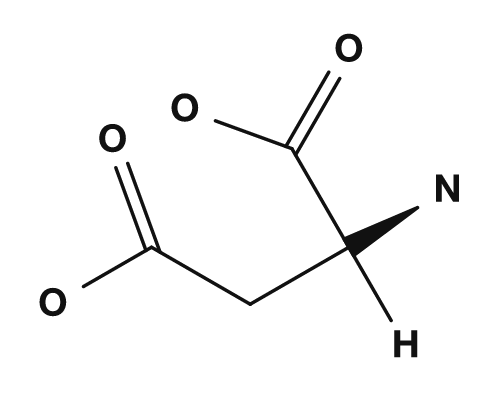
|
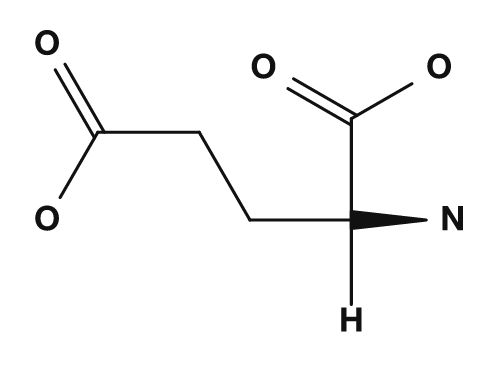
|
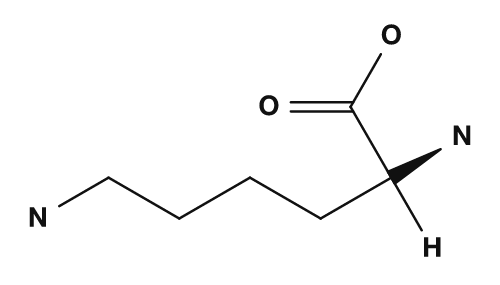
|
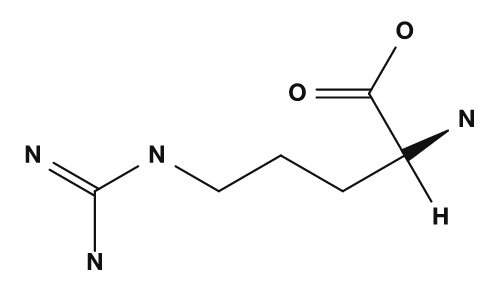
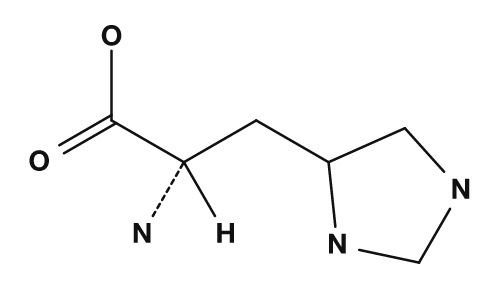
| アルギニン | ヒスチジン |
|---|---|
|
|
構造式から電荷を考える
構造式で等電点を考えるときは,電荷を持ちうる部分を探すことが第一歩です.
- アミノ基とカルボキシ基を確認する
- 側鎖に酸性・塩基性の官能基があるか確認する
- アスパラギン酸・グルタミン酸 → 側鎖のカルボキシ基
- リシン → 側鎖のアミノ基
- アルギニン → グアニジノ基
- ヒスチジン → イミダゾール環
等電点の応用
等電点は,タンパク質の分離や精製でも重要です.分子の正味電荷がpHによって変わるため,電気泳動やイオン交換クロマトグラフィーなどで利用されます.
- pHが等電点より低い → 分子は正に帯電しやすい
- pHが等電点より高い → 分子は負に帯電しやすい
PMC掲載論文でも,タンパク質はpIより低いpHで正に,pIより高いpHで負に帯電すると説明されています.
まとめ
等電点とは,アミノ酸やタンパク質の正味電荷が0になるpHです.アミノ酸では,アミノ基,カルボキシ基,側鎖の電離状態がpHによって変わるため,電荷も変化します.構造式を見るときは,電荷を持ちうる官能基を探すことが等電点理解の第一歩です.