多くのアミノ酸は,立体異性体を持ちます.その理由は,α炭素がキラル中心になっているからです.キラル中心とは,4種類の異なる置換基が結合した炭素原子のことです.タンパク質を構成する多くのα-アミノ酸では,α炭素にアミノ基,カルボキシ基,水素原子,側鎖R基が結合しているため,キラル中心になります.NCBI Bookshelfでは,タンパク質構成アミノ酸はα-アミノ酸であり,グリシンを除いてα炭素にキラル中心を持つと説明されています.
D体とL体の表記
アミノ酸の立体化学でよく出てくる表記に,D体とL体があります.D/L表記は,グリセルアルデヒドを基準にした相対配置を表す方法です.タンパク質を構成する標準的なアミノ酸は,基本的にL-アミノ酸です.NCBI Bookshelfでも,タンパク質を構成する20種類のアミノ酸はすべてL異性体であると説明されています.
D/L表記とR/S表記の違い
D/L表記とR/S表記は同じものではありません.
| 表記体系 | 基準 | タンパク質構成アミノ酸 | 例外 |
|---|---|---|---|
| D/L表記 | グリセルアルデヒドを基準とした相対配置 | L体 | グリシン(キラル中心なし) |
| R/S表記 | CIP順位則による絶対配置 | S配置が多い | システイン(R配置) |
D/Lは歴史的な相対配置に基づく表記であり,R/SはCIP順位則に基づく絶対配置です.多くのL-アミノ酸はS配置を持ちますが,システインは側鎖に硫黄を含むため優先順位が変わり,例外的にR配置になります.NCBI Bookshelfでも,グリシンとシステインを除く標準アミノ酸はR/S表記ではS配置であり,システインは硫黄を含むR基のためR配置になると説明されています.
構造式でのキラル中心の確認
構造式でキラル中心を見つけるときは,α炭素に注目します.その炭素に結合している4つの置換基がすべて異なっていれば,キラル中心です.
| アミノ酸 | α炭素の置換基 | キラル中心 |
|---|---|---|
| アラニン | NH2,COOH,H,CH3 |
あり(4種類すべて異なる) |
| グリシン | NH2,COOH,H,H |
なし(水素が2つ) |
| アラニン | グリシン | システイン |
|---|---|---|
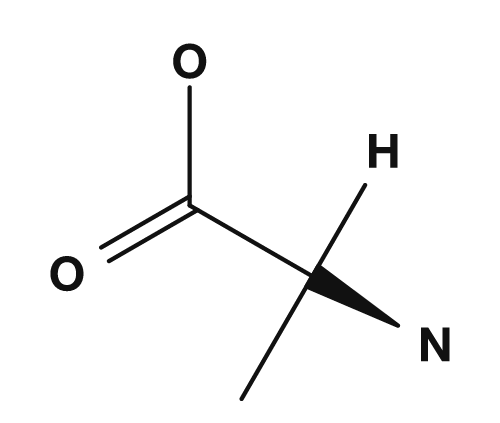
|
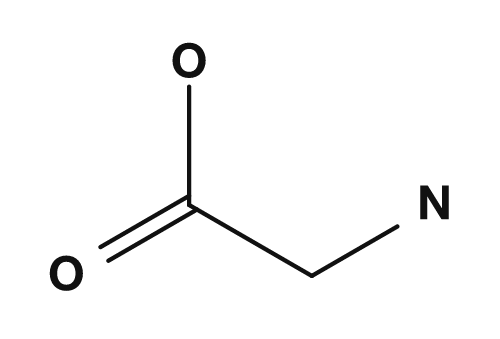
|
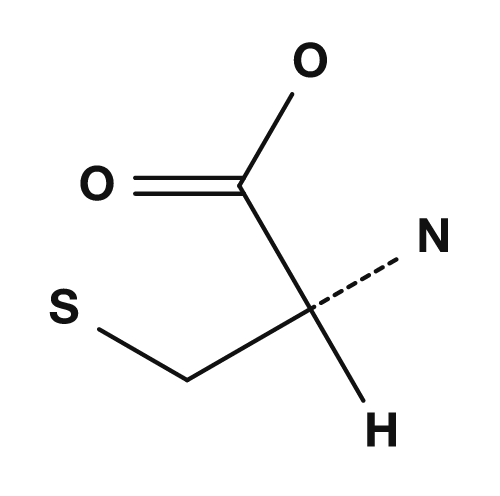
|
アラニンでは,α炭素に NH2,COOH,H,CH3 が結合しています.4つがすべて異なるため,アラニンはキラルです.一方,グリシンではR基が水素です.α炭素には NH2,COOH,H,H が結合するため,4種類にならず,キラル中心を持ちません.PubChemでも,グリシンは側鎖が水素原子であり,唯一のアキラルなタンパク質構成アミノ酸と説明されています.
D体・L体と旋光方向
D体とL体は鏡像異性体(エナンチオマー)の関係にあります.同じ分子式,同じ結合関係を持っていても,空間配置が鏡像関係で重ね合わせられない場合,エナンチオマーと呼ばれます.アミノ酸では,この立体配置の違いが生体分子との相互作用に大きく影響します.生体内の酵素や受容体は立体構造を持つため,L体とD体を区別できます.
アミノ酸のD/L表記を学ぶときに大切なのは,「Lだから左旋性」「Dだから右旋性」と単純に考えないことです.D/L表記は旋光方向を直接表すものではありません.旋光方向は実験的に測定される性質であり,+ や - で表されます.D/Lは構造上の相対配置を表す記号です.
構造式学習のポイント
構造式の学習としては,まずα炭素に4種類の置換基があるかを確認することが第一歩です.
- α炭素に4種類の置換基があるかを確認する
- グリシンは例外的にキラル中心を持たない
- タンパク質を構成するアミノ酸は基本的にL体
- D/L表記とR/S表記は別の表記体系
- システインはL体でありながらR配置という例外
まとめ
多くのアミノ酸は,α炭素に4種類の置換基を持つためキラルです.タンパク質を構成する標準アミノ酸は基本的にL体であり,グリシンだけはα炭素に同じ水素が2つ結合するためキラル中心を持ちません.D/L表記とR/S表記は別の体系であり,特にシステインは例外として理解しておく必要があります.