アミノ酸は,単独で存在するだけでなく,互いにつながることでペプチドやタンパク質を作ります.このときアミノ酸どうしをつなぐ結合がペプチド結合です.NCBI Bookshelfでは,タンパク質はアミノ酸がペプチド結合でつながった鎖であり,アミノ酸配列が一次構造を決めると説明されています.
| グリシン | アラニン |
|---|---|
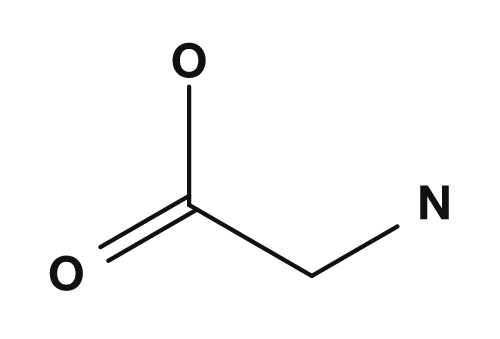
|
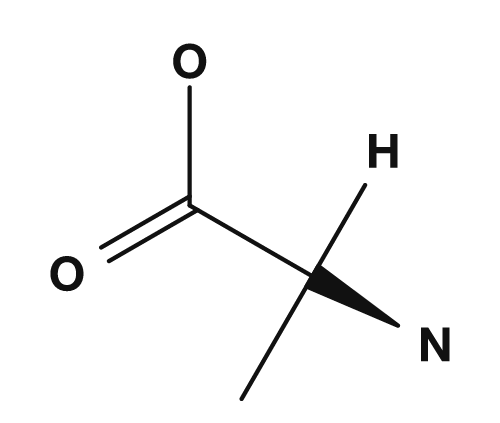
|
ペプチド結合の形成
ペプチド結合は,一方のアミノ酸のカルボキシ基と,もう一方のアミノ酸のアミノ基が反応してできるアミド結合です.反応では水が1分子抜けるため,縮合反応として説明されます.構造式で表すと,次のような部分構造になります.
-CO-NH-
この -CO-NH- がペプチド結合です.カルボン酸とアミンが結合してアミドになる構造なので,ペプチド結合はアミド結合の一種と考えることができます.NCBI BookshelfのPeptideの項目では,ペプチドは2〜50個のアミノ酸が縮合反応によって共有結合でつながった短い鎖であると説明されています.
ペプチド鎖の種類
アミノ酸がつながる数によって,次のように呼び方が変わります.Molecular Biology of the Cellでは,タンパク質は20種類のアミノ酸が共有結合性のペプチド結合でつながった長い鎖であると説明されています.
| 名称 | アミノ酸の数 |
|---|---|
| ジペプチド | 2 |
| トリペプチド | 3 |
| オリゴペプチド | 数個〜十数個程度 |
| ポリペプチド | それ以上 |
| タンパク質 | 長いポリペプチド鎖が折りたたまれたもの |
ペプチド結合の特徴:部分的な二重結合性
ペプチド結合の重要な特徴は,単なる単結合とは異なり,部分的な二重結合性を持つことです.これは,アミドの窒素の孤立電子対がカルボニル基と共鳴するためです.その結果,ペプチド結合周辺は平面性を持ち,回転が制限されます.この性質は,タンパク質の立体構造を考えるうえで非常に重要です.
ペプチド結合の主な特徴:
- アミド結合(
-CO-NH-)の一種 - 縮合反応(水分子の脱離)によって形成される
- 部分的な二重結合性を持つ
- 結合周辺は平面性を持ち,回転が制限される
N末端とC末端
ペプチド鎖には方向性があります.
| 末端 | 残る官能基 | 読み方の基準 |
|---|---|---|
| N末端 | アミノ基(-NH2) |
アミノ酸配列の書き始め |
| C末端 | カルボキシ基(-COOH) |
アミノ酸配列の書き終わり |
タンパク質のアミノ酸配列は,通常N末端からC末端に向かって表記されます.この方向性を理解しておくと,ペプチドやタンパク質の構造式を読みやすくなります.
構造式でのペプチド結合の見分け方
ペプチド結合を構造式で見分けるには,-CO-NH- の部分を探します.カルボニル炭素に窒素が結合しているため,アミド構造と同じです.ただし,その両側にアミノ酸由来のα炭素がつながっている場合,それはペプチド結合として扱われます.
生物学的な重要性
ペプチド結合は,生物にとって非常に重要です.酵素,抗体,ホルモン,構造タンパク質など,多くの生体分子はアミノ酸がペプチド結合でつながることで作られています.MedlinePlusでも,アミノ酸はタンパク質を作り,体組織の成長や修復などに使われると説明されています.
まとめ
ペプチド結合は,一方のアミノ酸のカルボキシ基と,もう一方のアミノ酸のアミノ基が縮合してできる -CO-NH- 結合です.ペプチド結合はアミド結合の一種であり,部分的な二重結合性を持つため,タンパク質の立体構造にも影響します.アミノ酸がペプチド結合でつながることで,ペプチドやタンパク質が作られます.